Фотохимический распад - молекула
Cтраница 1
Фотохимический распад молекулы происходит после некоторого времени жизни Т; в дискретном состоянии. Связь между диффузностью и фотохимическим распадом была впервые установлена Бонхеффером и Фаркашем [129], которые показали, что фотораспад NH3, возникающий при поглощении света в области диффузных полос около 2100 А ( фиг. [1]
Возможны три основных способа фотохимического распада молекул. В отдельных случаях может иметь место прямая фото-диссоциация в результате перехода молекулы в состояние типа S2 ( см. рис. 47), в котором притяжение между атомами сменяется отталкиванием. [2]
Аддитивную полимеризацию инициируют свободные радикалы, образующиеся при термическом или фотохимическом распаде молекул подходящего инициатора. [3]
При этом получаются довольно длинные цепи-порядка 1000 звеньев на один атом хлора, образовавшийся в результате фотохимического распада молекулы хлора. [4]
При этом получаются довольно длинные цепи - порядка 1000 звеньев на один атом хлора, образовавшийся в результате фотохимического распада молекулы хлора. [5]
Так, например, у альдегидов, кетонов и карбоновых кислот центром возбуждения является общая всем этим соединениям группа СО, что следует из положения их длинноволнового спектра. Разрывающимися связями при фотохимическом распаде молекулы здесь могут быть как связи с атомом С этой группы, так и связи в других группах, как это следует из анализа продуктов фотохимического разложения альдегидов, кетонов и кислот. [6]
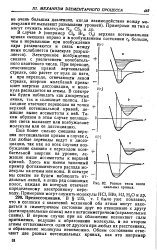 |
Разные типы потен циальных кривых. [7] |
Еще более сильно смещена верхняя потенциальная кривая в случае с, где любые переходы ведут к диссоциации, так как во всех случаях возбуждение связано с переходом коле-бательной энергии на уровни, лежащие выше ассимптоты к верхней кривой. Здесь мы имеем типичный пример фотохимического распада молекулы на атомы или ионы. В спектре мы совсем не будем наблюдать отдельных линий, а лишь ряд сплошных полос, каждая из которых отвечает определенному электронному переходу. [8]
В более поздний период изменение состава атмосферы и превращение ее из восстановительной в окислительную было связано с обогащением атмосферы кислородом. Появление кислорода в добиологическую эру могло быть обусловлено фотохимическим распадом молекул воды в верхних слоях атмосферы; позже, как указал В. И. Вернадский, поставщиком кислорода стали фотосинтезирующие организмы. [9]
Наряду со структурой спектра, далеко не всегда в достаточной степени изученной, о большой распространенности предиссоциационного распада свидетельствуют также данные, относящиеся к взаимоотношению между центром возбуждения молекулы и разрываемыми связями. Так, например, у альдегидов, кетонов и карбоновых кислот центром возбуждения является общая всем этим соединениям группа / СО. Разрывающимися связями при фотохимическом распаде молекулы здесь могут быть как связи с атомом углерода этой группы, так и связи в других группах, как это следует из анализа продуктов фотохимического разложения альдегидов, кетонов и кислот. [10]
Многие особенности образования и поведения радикалов и ионов в твердых замороженных веществах связаны с наличием клеточного эффекта, обнаруженным в свое время для реакций в жидкой фазе. Наиболее ярко клеточный эффект проявляется в фотохимических процессах. В вязких жидкостях возникающие при фотодиссоциации молекулы два радикала в первый момент находятся друг около друга, как бы в клетке, и лишь в результате последующей диффузии дают две независимых частицы. Клеточный эффект влияет на эффективность воздействия света при фотохимическом распаде молекул в твердой фазе. Получение количественных данных о клеточном эффекте при низких температурах довольно сложно. [11]
Страницы: 1