Кислый расплав
Cтраница 1
Кислые расплавы используют для разложения нерастворимых в кислотах оксидов металлов основного или амфотерного характера, например оксиды титана, хрома, кобальта, никеля, железа, алюминия и пр. Типичным расплавом этого типа является пиро-сульфат калия. [1]
Остаточный сравнительно кислый расплав, богатый силикатами, затвердевает, образуя сначала полевые шпаты и кварц, а затем пегматиты, несущие литий, бериллий, торий, ниобий, тантал. Из газов и паров возникают месторождения олова, вольфрама и других металлов. Из перегретых под давлением водных растворов в трещинах горных пород выделяются гидротермальным путем сульфиды железа, сурьмы, цинка, ртути, мышьяка, карбонаты, золото, серебро и другие вещества. [2]
Тигли из спеченных корунда или берилла почти непригодны для кислых расплавов. В то время как K2S2O7 едва заметно разрушает глазурованный фарфор или кварцевое стекло, из тигля из спеченного корунда в течение часа в раствор переходит около 1000 мг материала. Тигли из А12О3 неприменимы для всех фторсодержащих расплавов. Однако тигли из спеченной шпинели не взаимодействуют с ВаС12 при 1300 даже в течение недели. [3]
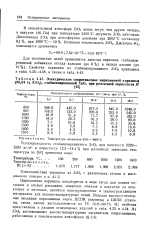 |
Электрическое сопротивление циркониевой керамики ( 99 94 о / о ZrO, стабилизированной СаО, при различной пористости П. [4] |
Циркониевая керамика используется в виде тигля для плавки металлов и кислых расплавов, защитных обмазок и покрытий на огнеупорах и металлах, является конструкционным и теплоограждающим материалом для высокотемпературных печей. [5]
Реакция (4.30) начинается при температурах около 1000 С и протекает главным образом в кислых расплавах. С повышением температуры реакция сдвигается вправо, а при понижении происходит диспропорционирование субфторида с образованием мелкодисперсного металлического алюминия и фторида алюминия. [6]
Оксиды таких элементов часто как струны проходят через всю толщину окалины А12О3 и легко вступают в реакцию с кислым расплавом осадка. В сплаве, однако, существуют и другие слабые места, через которые соль может проникать через оксидную пленку [52], так что само по себе присутствие в сплаве кислоро-до-активных элементов не слишком заметно сказывается на снижении длительности начальной стадии коррозии. [7]
При щелочном сплавлении в качестве плавней применяют карбонаты, гидрокснды, бораты щелочных металлов и их смеси, а также обладающие окислительным действием пероксиды. Реже используют кислые расплавы, например пиросульфат и гндросульфат калия, оксид бора. Если твердый реагент имеет очень высокую температуру плавления ( например, оксид или карбонат кальция), то проводят не сплавление, а спекание. Разложение этим методом ведут обычно при более высоких температурах ( до 1000 С), при которых реакции, протекающие в спекаемой смеси, происходят более интенсивно. [8]
С расплавами щелочных солей не приходится иметь дело при высоких температурах вследствие их легкоплавкости. Фарфор применим лишь в случае нейтральных или кислых расплавов. Плавление NaOH при 400 в тигле из спеченного корунда ( чаще всего применяемого размера) в течение часа вызывает потерю в весе около 50 мг. В процессе плавления смеси Na2CO3 и KNO3 при 700 за I час в реакцию вступает около 75 мг корунда. [9]
Присутствие в смесях СаО с алюмосиликатами окиси магния не сказывается существенно на последовательности минералообразования; лишь при недостатке СаО в зоне реакции в интервале температур от 1473 до 1573 К могут образоваться окерманит ( 2CaO - MgO - 2SiO2) и твердые растворы окерманита и геленита - мелилиты. Полевые шпаты при реакции с СаО разлагаются, начиная примерно с 1173 К, с выделением соединений типа лейцита и кислого расплава. [10]
При твердофазном кислом флюсовании обычные защитные оксиды могут уничтожаться путем их необратимого или обратимого, с последующим выпадением в осадок уже в виде незащищающих оксидов, растворения в расплаве. Мисра [40] исследовал коррозию никелевых суперсплавов с молибденом под слоем Na2SO4 при 950 С и пришел к выводу, что твердофазное кислое флюсование в этом случае протекает по механизму, близкому к предложенному Лутра [31-34], согласно которому в кислом расплаве происходит образование ионов Ni2 и выделение NiO на границе раздела расплава с газом. Формирование сплошных пленок А12О3 и Сг2О3 на поверхности сплава в этом случае невозможно из-за обеднения сплава никелем. [11]
Большинство других элементов, присутствующих в суперсплавах и материалах покрытий этих сплавов, не оказывают сколь-нибудь значительного влияния на процесс газофазного кислого флюсования. Исключительно высоким сопротивлением кислотному флюсованию обладает окалина диоксида кремния, формирующаяся на поверхности некоторых покрытий. Эти оксиды слабо растворимы в кислых расплавах ( рис. 12.12) и такие защитные окалины часто образуются на сплавах с достаточно высоким содержанием кремния. Использованию таких окалин как части системы защиты сплавов препятствует, однако, их высокая чувствительность к коррозионной деградации за счет основного флюсования. [12]
CaO и А12Оз отсасываются в виде силикатных расплавов в наиболее далекие от рабочей поверхности слои динаса, тогда как окислы железа скопляются в рабочей толще динаса. Первые расплавы, согласно ранее приведенному, должны иметь большее поверхностное натяжение, чем железистые расплавы, что в соответствии с изложенным должно обеспечивать более быстрое всасывание расплавов, образуемых СаО и АЬОз с кремнеземом. FeO - СаО - SiC2 показывают, что в области кислых расплавов увеличение SiC2 снижает ож. [13]
По своим химическим свойствам окись бериллия занимает промежуточное место между А12О3 и MgO, являясь слабоосновным огнеупором. Окись бериллия довольно чувствительна к влиянию различных окислов, шлаков и расплавов стекла, особенно по отношению к кислым расплавам. Поэтому тигли из спеченной ВеО непригодны для плавки стекла. [14]
В гранитоидах содержания гафния несколько возрастают, достигая максимальной величины ( до 9 г / т) в кислых породах Барангуловского массива. Значения Zr / Hf отношения снижаются и колеблятся в более узких пределах ( 2 - 26), что определяется сравнительно монотонным распределением обоих элементов в гранитах при большей обо-гащенности их гафнием. Учитывая то, что главным минералом-концентратором гафния и циркония в гранитах обычно является циркон, можно допустить, что в процессе образования генетически связанных пород габбро-гранитного комплекса остаточные кислые расплавы и кристаллизующиеся из них цирконы, по-видимому, несколько обогащались гафнием. [15]
Страницы: 1 2