Оставшийся расплав
Cтраница 2
После его практически полного выделения процесс электролиза прекратится, так как для разложения оставшихся солей КС1 и СаС12 необходима более высокая разность потенциалов. Оставшийся расплав будет очищен от ионов магния и свинца. [16]
Возможны и другие способы выделения дифенилолпропана из реакционной массы и его очистки. Органический слой отделяют от водного и промывают водой. Затем органический слой перегоняют в вакууме для отделения воды, хлорбензола, фенола. Оставшийся расплав продувают паром при 170 - 175 С и остаточном давлении 10 мм рт. ст. для удаления промотора, содержащего серу. Способ рекомендуется лишь в том случае, если на синтез берут избыток фенола по сравнению со стехиометрическим. Вследствие того что растворитель содержит большое количество непрореагировавшего фенола, выделение из него чистого дифенилолпропана кристаллизацией затруднено, и поэтому применяется вакуумная отгонка. [17]
Оставшийся расплав будет очищен от ионов магния и свинца. [18]
Предложен [3] двухступенчатый реактор, в первую зону которого поступает расплав серы, трехоксид мышьяка и хлор. Температуру поддерживают выше температуры кипения хлорида и ниже температуры кипения расплава. Оставшийся расплав, непрореагировавшую окись и дополнительное количество серы подают во вторую зону для дохлорирования. [19]
Когда будет достигнута точка g, система находится при температуре начала кристаллизации, но в точке g имеется только одна фаза. Малейшее понижение температуры вызывает образование ничтожного количества кристаллов вещества А. Состав оставшегося расплава обогащается веществом В, и для выделения следующих кристаллов А необходимо дальнейшее понижение температуры. [20]
 |
Формы тиглей для выращивания кристаллов из расплава. [21] |
Один из способов заключается в следующем. В тигле определенной формы ( рис. 25) вначале выращивают часть кристаллов. К оставшемуся расплаву добавляют р-примесь в таком количестве, чтобы изменился тип проводимости. Для точного ( до 5 - 10 %) взвешивания доли микрограмма п - или р-примеси ее берут в виде сплава с полупроводником, содержащим десятые или сотые доли процента заданной примеси. [22]
При дальнейшем снижении температуры из расплава выпадают уже кристаллы компонентов А и В, а состав остающегося расплава изменяется в соответствии со значениями точек, расположенных на линии е Е до тех пор, пока он численно не станет равным эвтектическому составу Е при Те. Дальнейшее снижение температуры сопровождается полной кристаллизацией оставшегося расплава. [23]
Углерод создает восстановительную среду, что сильно влияет на образование жидкой фазы. Углерод препятствует капиллярному проникновению шлака и замедляет реакции между шлаком и огнеупором из-за своей плохой смачиваемости шлаками. Взаимодействие углерода со шлаками зависит от основности шлака. Если основность высокая, то углерод восстанавливает ионы тяжелых металлов, и оставшийся расплав при этом затвердевает. При низкой основности шлака эта реакция не происходит. Углерод не смачивается расплавом кислых шлаков. [24]
Теперь мы хотим выяснить, что получится, если взять два куска германия или кремния с неодинаковыми внутренними характеристиками, скажем с разным количеством примеси, и приложить их друг к другу, чтобы возник переход. Начнем с того, что именуется р-я-переходом, когда с одной стороны границы стоит германий р-типа, а с другой - германий п-типа ( фиг. Практически не очень удобно прикладывать друг к другу два разных куска германия и добиваться однородности контакта между ними на атомном уровне. Вместо этого переходы делают из одного кристалла, обработанного в разных концах по-разному. Один из приемов состоит в том, чтобы после того, как из расплава была выращена половинка кристалла, добавить в оставшийся расплав подходящую присадку. [25]
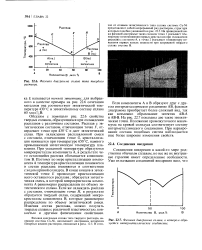 |
Фазовая диаграмма сплава типа твердого раствора.| Фазовая диаграмма сплава, в котором образуется интерметаллическое соединение. [26] |
Обсудим с помощью рис. 22.6 свойства твердых сплавов, образующихся при охлаждении расплавов с различным составом. Расплав с эвтектическим составом, отвечающим точке F, отвердевает точно при 430 С и дает эвтектический сплав. При охлаждении расплавленной смеси с составом, отвечающим точке G, кристаллизация начинается при температуре 650 С, намного превышающей эвтектическую температуру плавления. При указанной температуре образуются микрокристаллы компонента А, в результате чего остающийся расплав обогащается компонентом В. Поэтому по мере кристаллизации компонента А температура кристаллизации понижается и состав расплава изменяется в соответствии с ходом кривой солидуса. В конце концов в эвтектической точке Е происходит кристаллизация всего оставшегося расплава; образуется эвтектическая смесь, в которой микрокристаллы компонента А равномерно распределены по объему эвтектического сплава. Если же охлаждать расплав с составом, отвечающим точке Я, в результате образуется твердый сплав, содержащий микрокристаллы компонента В, которые равномерно распределены по объему эвтектической смеси. Изменяя состав расплава, можно получать твердые сплавы с различной пластичностью, ковкостью и другими физическими свойствами. [27]
Точное установление поверхности ликвидус, конечно, включает определение составов слитков, с которых снимались кривые охлаждения. Может быть также применен описанный выше метод, в котором небольшая часть расплава выливается в холодную форму незадолго перед тем, как достигается температура остановки. Этот метод имеет определенное преимущество, так как получающийся слиток имеет состав образца, с которого снята кривая охлаждения; таким образом, может значительно уменьшиться число требующихся химических определений. Стоимость химических анализов при построении тройной диаграммы очень велика. Нужно сделать вое возможное, чтобы использовать данные одного анализа для нескольких целей. Если сплавы обладают повышенной химической активностью и не могут быть отлиты на воздухе, то можно для отбора небольших порций металла приспособить установку, показанную на рис. 36, а с оставшегося расплава снимать кривые охлаждения. [28]
Пользуясь правилом рычага, можно для каждой точки найти весовые количества равновесных жидких слоев. При этом из расплава начнут выделяться кристаллы вещества В. Число фаз в системе станет равным трем ( две жидких и одна твердая), и, следовательно, система будет находиться в инвариантном равновесии. В результате этого процесса состав как жидкости F, так и жидкости Е все время остается неизменным, и мы будем наблюдать лишь постепенное уменьшение количества жидкости. В С оставшийся расплав затвердевает, как эвтектика. [29]
При этом в слое / содержание компонента В уменьшается, а в слое / - растет. Изменяется и отношение весовых количеств жидких слоев. Пользуясь правилом рычага, можно для каждой точки найти весовые количества равновесных жидких слоев. При этом из расплава начнут выделяться кристаллы вещества В. Число фаз в системе станет равным трем ( две жидких и одна твердая) и, следовательно, система будет находиться в инвариантном равновесии. В результате этого процесса состав как жидкости F, так и жидкости Е все время остается неизменным, и мы будем наблюдать лишь постепенное уменьшение количества жидкости. Первым исчезает расплав F и останутся две фазы - расплав Е и кристаллы В. В С оставшийся расплав затвердевает, как эвтектика. [30]
Страницы: 1 2