Большая величина - энергия
Cтраница 2
Они отличаются повышенной нагревостойкостью вследствие большой величины энергии связи углерод - фтор. [16]
Характерной особенностью столба тлеющего разряда являются большие величины энергии электронов, значительно превосходящие среднюю энергию газовых молекул. [17]
Галоидные соли металлов II группы имеют большую величину энергии кристаллических решеток, чем соответствующие галоидные соли металлов I группы, что также отвечает большему поверхностному натяжению расплавленных хлористых и фтористых солей металлов II группы. [18]
 |
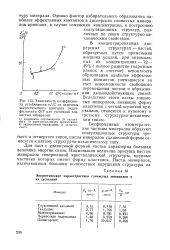
Зависимость выхода полимера от продолжительности полимеризации триоксана в твердой фазе. [19] |
Предполагается, что это связано с большой величиной энергии ионизации кристаллического иода. [20]
Для паст с удлиненной формой частиц характерна большая величина энергии связи. Наименьшая величина присуща пастам минералов совершенной кристаллической структуры, крупные частички которых имеют форму пластинок. [22]
Отсюда следует, что для соединения с большой величиной энергии кристаллической решетки разрушение решетки может стать чрезвычайно невыгодным процессом и реакция будет протекать по другому механизму. Сопоставление энергий кристаллических решеток окислов II и IV групп показывает, что для первых она колеблется от 700 до 1000 ккал / молъ, а для вторых она значительно больше и составляет 2500 - 3000 ккал / молъ. [23]
Они приведены в табл. 26, Несмотря на большие величины энергий реакций, даваемые этими расчетами, часто утверждают, что субгалогениды щелочных металлов, серебра, а также щелочноземельных металлов могут образовываться при нагревании металла в присутствии нормального галогенида или при электролизе последнего в расплавленном состоянии. Однако некоторые авторы считают, что такие субгалогениды скорее представляют собой раствор металла в нормальном галогениде. [24]
Относительные величины энергии водородной связи и дисперсионной энергии объясняют большую величину энергии сублимации и более высокую точку плавления льда по сравнению с соединениями, подобными метану, в которых когезионные силы обладают в основном дисперсионным характером. С другой стороны, лед имеет меньшую энергию сублимации и более НИЗКУЮ точку плавления, чем ковалентные кристаллы, такие, как алмаз. Относительные значения прочности водородных связей и дисперсионных сил помогают также объяснить открытую структуру льда. Существование двух водородных связей в одной молекуле энергетически более выгодно, чем увеличение дисперсионных взаимодействий, которое могло бы иметь место, если бы лед не имел водородных связей и характеризовался более плотной упаковкой молекул. [25]
Эти испытания не дают ничего нового, так как при большой величине энергии каждого удара они приближаются по результатам к ударной пробе, а при очень малой-к статической усталости. [26]
Кальциевые монтмориллониты прочнее связывают воду, чем натриевые, и обладают большей величиной энергии связи, что подтверждается при определении теплоты смачивания. Однако диффузный слой ионов кальциевых глин меньше, чем у натриевых, поэтому у них не наблюдается пептиза-ции частиц, что характерно для натриевых глин. [27]
Кальциевые монтмориллониты прочнее связывают воду, чем натриевые, и обладают большей величиной энергии связи. Однако диффузный слой ионов кальциевых глин меньше, чем натриевых, поэтому для них характерно явление пептизации, определяющее особенности коагуляционно-тиксотропной структуры в суспензии. [28]
Следует отметить, что более отрицательным значениям потенциала металлического электрода соответствуют и большие величины энергии перехода данного металла в виде катионов в раствор. [29]
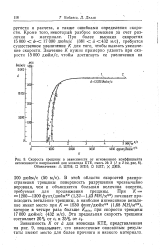 |
Скорость трещины в зависимости от мгновенного коэффициента интенсивности напряжений для эпоксида К. ТЕ, смесь № 3 ( / и 2см. 8. Обозначения. Д ЦПН. D ЭПН. О НЛТ. X ДКБ. [30] |
Страницы: 1 2 3 4