Распределение - индий
Cтраница 1
Распределение индия в процессах пирометаллургической переработки руд определяется тем, что как сам металлический индий, так и его высший окисел 1п2О3 обладают весьма малым давлением пара. Поэтому индий малолетуч в сильноокислительной среде и в процессах окислительного обжига, как правило, остается в огарке. Также в сильновосстановительной среде, когда индий восстанавливается до металла, его переход в возгоны незначителен. Это соединение устойчиво только в парах и при конденсации диспропорционирует на металл и окись индия. При получении цинка пирометаллургическим путем индий распределяется примерно поровну между черновым цинком и раймовкой. [1]
Распределение индия в процессах пирометаллургической переработки руд обусловливается тем, что как сам металл, так и его высший окисел 1п2О3 обладают весьма малым давлением пара. Поэтому индий при окислительном обжиге, как правило, остается в огарке. В скльно-восстановительной среде, когда он восстанавливается до металла, его переход в возгоны незначителен. [2]
Распределение индия в процессах пирометаллургической переработки руд обусловливается тем, что как сам металл, так и его высший окисел 1п2О3 обладают весьма малым давлением пара. Поэтому индий при окислительном обжиге, как правило, остается в огарке. В сильновосстановительной среде, когда он восстанавливается до металла, его переход в возгоны незначителен. [3]
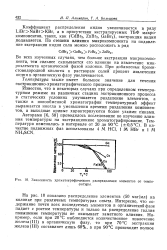 |
Зависимость хроматопрафичеокого. распределения элементов от температуры. [4] |
Коэффициент распределения индия увеличивается в ряду LiBrNaBrKBr, а в присутствии экстрагируемых ТБФ макрокомпонентов, таких, как ( CdBr2, ZnBr2, GaBr3), экстракция индия подавляется. [5]
Величины коэффициентов распределения индия, кальция, магния, марганца ( II) при данных рН растворов значительно больше нуля. [6]
Таким путем было подтверждено установленное другим методом значение коэффициента распределения индия ( / С0 1) в арсениде галлия. [7]
С другой стороны, известно [6, 19-22], что образование ионных ассо-циатов в органической фазе приводит к увеличению коэффициентов распределения с повышением концентрации экстрагируемого элемента. Естественно поэтому считать, что причиной повышения коэффициента распределения индия ( см. рис. 1) с ростом его концентрации является именно ассоциация ионов экстрагируемого соединения в органической фазе. [8]
С другой стороны, известно [6, 19-22], что образование ионных ассоциатов в органической фазе приводит к увеличению коэффициентов распределения с повышением концентрации экстрагируемого элемента. Естественно поэтому считать, что причиной повышения коэффициента распределения индия ( см. рис. 1) с ростом его концентрации является именно ассоциация ионов экстрагируемого соединения в органической фазе. [9]
Коэффициенты распределения цинка в отсутствие индия практически не зависят от концентрации кислоты. Особенно резко коэффициент распределения цинка растет при концентрации НВг свыше 5 М, где коэффициент распределения индия достигает максимального значения. [10]
Данное выше значение константы, по-видимому, завышено, так как оно определялось из данных растворимости оксихинолята индия в растворах, содержащих спирт, в которых растворимость этого соединения выше, чем в воде. Кроме того, в приведенном выше выражении не учитываются промежуточные ( заряженные) комплексы индия с 8-оксихинолином, а такие молекулы обычно существуют в данном интервале кислотности. Поэтому приведенное выражение, описывающее распределение индия между двумя фазами, следует рассматривать как грубо приближенное. [11]
По мере повышения температуры и приближения ее к ТА х падает. Понижение же температуры невыгодно - х в растет. Это именно наблюдалось в работе [75] ( см. рис. VI.29) для коэффициента распределения индия и сурьмы в германии. [12]
Страницы: 1