Распределение - микрокомпонент
Cтраница 2
А коэффициент распределения микрокомпонента В не зависит от его концентрации. Это означает, что поглощение ионов микрокомпонента прямо пропорционально его концентрации в растворе, откуда следует, что при очень малых концентрациях изотерма сорбции линейна. Этот факт, весьма важный для хроматографии, экспериментально подтвержден Майером и Томпкинсом [100] и рядом других авторов. [16]
Для изучения распределения микрокомпонента РЬС12, меченного ThB, между раствором и кристаллами ВаС12 используется метод изотермического снятия пресыщения. [17]
При изучении распределения микрокомпонента в системе раствор - твердая фаза было установлено, что коэффициент кристаллизации возрастает с уменьшением активности макрокомпонента и падает с уменьшением активности микрокомпонента в жидкой фазе. [18]
Количественные закономерности распределения микрокомпонента между твердой и жидкой фазами были изучены В. Г. Хло-пиным и его учениками. [19]
При изучении распределения микрокомпонента между кристаллами и раствором удобно пользоваться формулой ( 106) ( стр. [20]
При изучении распределения микрокомпонента между различными фазами очень большую роль играет его состояние, или ф о pjvt а нахождения. В предыдущей главе мы рассмотрели состояние микроколичеств радиоактивных изотопов в жидкой, газовой и твердой фазах и убедились, что сведения по этому вопросу очень ограничены. Поэтому установление законов поведения микрокомпонентов пока производилось на примере простейших систем, когда микрокомпонент находится в простой ионной форме. Однако в соответствующих условиях должна быть учтена возможность образования коллоидов или комплексных соединений. [21]
При изучении распределения микрокомпонента между различными фазами очень большую роль играет его состояние, или форма н а х о ж д е н и я. В предыдущей главе мы рассмотрели состояние микроколичеств радиоактивных изотопов в жидкой, газовой и твердой фазах и убедились, что сведения по этому вопросу очень ограничены. Поэтому установление законов поведения микрокомпонентов пока производилось на примере простейших систем, когда микрокомпонент находится в простой ионной форме. Однако в соответствующих условиях должна быть учтена возможность образования коллоидов или комплексных соединений. [22]
Величина практического коэффициента распределения микрокомпонента зависит, кроме того, от методов и условий проведения процесса выделения из раствора твердой фазы, влияющих на отклонение от равновесия для конечной температуры кристаллизации. Если имеют дело с элементами с переменной валентностью, обычно широко применяется предварительное окисление или восстановление для превращения изоморфных компонентов п неизоморфные. [23]
Экспериментальное изучение зависимости распределения микрокомпонента между кристаллической и жидкой фазами от концентрации катиона макрокомпонента при практически постоянной концентрации общего аниона может быть выполнено только при использовании метода изотермического снятия пересыщения соли основного вещества. В этом случае смешанные кристаллы образуются в результате обмена в твердой фаз одного катиона макро-компонента на один ион микрокоипояента с соответствующей перестройкой анионной части кристаллической решетки из-за требования электронейтральности решетки в целом. [24]
Другим предельным случаем распределения микрокомпонента по объему кристаллов при сокристаллизации является так называемое логарифмическое распределение. Оно наступает, когда осадок выделяется из слабо пересыщенного раствора путем снятия пересыщения на заранее внесенных затравках. Соблюдение всех этих условий приводит к тому, что в любой момент времени поверхность кристаллов находится в равновесии с жидкой фазой, и в растворе отсутствуют градиенты концентраций. [25]
Какая известна закономерность распределения микрокомпонента, кроме закона Хлопина, и при каких условиях она осуществляется. [26]
Проведенные исследования процесса распределения микрокомпонентов между расплавом и твердой изоморфной и неизоморфной фазами привели к установлению ряда закономерностей, которые, с одной стороны, свидетельствуют о наличии большой аналогии в поведении микрокомпонентов в расплавах и в растворах при процессе распределения, а, с другой стороны, указывают на определенную специфику поведения распределяющихся микрокомпонентов в расплавленных солях при высоких температурах. [27]
Наиб, важны особенности распределения микрокомпонента между фазами гетерог. В случае двух фаз - пара и жидкости-распределение микрокомпонента обычно подчиняется Генри закону. Если в первоначально гомогенной системе ( газообразной или жидкой) формируется ( или вносится в готовом виде) твердая фаза, то микрокомпонент переходит в твердую фазу в результате адсорбции и ( или) соосаждения. [28]
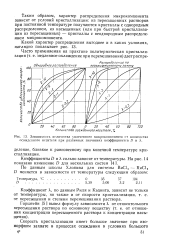 |
Зависимость количества увлеченного микрокомпонента ст количества осажденного носителя при различных значениях коэффициентов D и X. [29] |
Таким образом, характер распределения микрокомпонента зависит от условий кристаллизации: из пересыщенных растворов при постоянной температуре получаются кристаллы с однородным распределением, из насыщенных ( или при быстрой кристаллизации из пересыщенных) - кристаллы с неоднородным распределе-дием микрокомпонента. [30]
Страницы: 1 2 3 4