Распределение - прометий
Cтраница 1
Распределение прометия между кристаллами Sr ( N03) 2 и его расплавом в расплавах LiN03 и NaNOg изучено при 310, 330 и 350 С. [1]
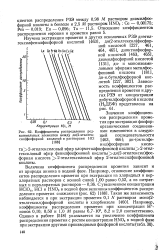 |
Коэффициенты распределения редкоземельных элементов между ди ( 2-этилгек-сил фосфорной кислотой и растворами НС1. [2] |
Величина коэффициента распределения прометия зависит и от природы аниона в водной фазе. Например, коэффициенты распределения прометия при концентрации Н - ионов 0 10; 0 50 и 1 0 М равны 6 7 - Ю2, 8 2 и 2 0 соответственно. [3]
Установлено, что в ряду кислот ( GO) 2PO ( ОН) - ( GO) GPO ( ОН) - G2PO ( ОН), где G - один и тот же алкил, коэффициент распределения прометия с появлением в экстрагенте одной С - Р - связи снижается примерно в 40 раз. [4]
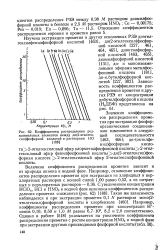 |
Коэффициенты распределения редкоземельных элементов между ди ( 2-этилгек-сил фосфорной кислотой и растворами НС1. [5] |
Величина коэффициента распределения прометия зависит и от природы аниона в водной фазе. Например, коэффициенты распределения прометия при концентрации Н - ионов 0 10; 0 50 и 1 0 М равны 6 7 - Ю2, 8 2 и 2 0 соответственно. [6]
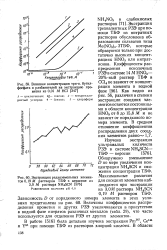 |
Влияние концентрации три-н. бутил-фосфата и разбавителей на экстракцию прометия из 0 01 М НС1.| Экстракция редкоземельных элементов 0 19 М раствором ТБФ в керосине из 3 0 М раствора NH4SCN. [7] |
Экстракция трехвалентных РЗЭ при по-мощи ТБФ из нитратных растворов обусловлена образованием сольватов типа Ме ( МО3) 3 - ЗТБФ, которые образуются только при достаточно высоких концентрациях НМО3 или нитрат-ионов. Как видно из рис. 56, различия в степени экстракции соседних элементов остаются постоянными в области концентрации НМО3 от 8 до 15 8 М и не зависят от порядкового номера элемента. Обнаружено уменьшение D по мере увеличения концентрации NH4SCN и снижения концентрации ТБФ. Величины коэффициентов распределения прометия и других РЗЭ увеличиваются в присутствии в водной фазе нитратов различных металлов ( табл. 29), что часто используется для отделения РЗЭ от других элементов. [8]
Хорошей иллюстрацией этому может явиться работа [39] по поглощению щелочноземельных, редкоземельных и трансурановых элементов катионитом. Было показано, что в случае щелочноземельных металлов кривая поглощения стронция имеет отчетливо выраженный минимум при 6 М соляной кислоте, кривая бария - пологий минимум, а на кривой радия наблюдается лишь точка перегиба. По мере увеличения концентрации соляной кислоты коэффициент распределения америция, как оказалось, закономерно уменьшается, по-видимому, вследствие образования отрицательно заряженных хлоридных комплексов. В то же время коэффициент распределения прометия при 7 М соляной кислоте проходит через минимум, что объясняется происходящей в концентрированных растворах кислоты дегидратацией ионов, приводящей, как было сказано выше, к увеличению сорбируемости иона. [9]
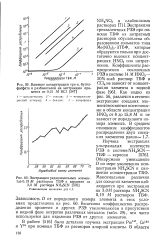 |
Влияние концентрации три-н. бутил - Аосфата и разбавителей на экстракцию прометия из 0 01 М НС1.| Экстракция редкоземельных элементов 0 19 М раствором ТБФ в керосине из 3 0 М раствора NH4SCN. [10] |
Экстракция трехвалентных РЗЭ при помощи ТБФ из нитратных растворов обусловлена образованием сольватов типа Ме ( Ш3) 3 - ЗТБФ, которые образуются только при достаточно высоких концентрациях НМО3 или нитрат-ионов. Как видно из рис. 56, различия в степени экстракции соседних элементов остаются постоянными в области концентрации НШ8 от 8 до 15 8 М и не зависят от порядкового номера элемента. Обнаружено уменьшение D по мере увеличения концентрации NH4SCN и снижения концентрации ТБФ. Максимальные различия для соседних элементов наблюдаются при экстракции из 3ОМ раствора NH4SCN 0 19 М раствором ТБФ. Величины коэффициентов распределения прометия и других РЗЭ увеличиваются в присутствии в водной фазе нитратов различных металлов ( табл. 29), что часто используется для отделения РЗЭ от других элементов. [11]
Страницы: 1