Распределение - растворенное вещество
Cтраница 2
Коэффициент распределения растворенного вещества между неподвижной жидкой фазой и газом-носителем изменяется экспоненциально с обратным значением абсолютной температуры, поэтому логарифм исправленного удерживаемого объема зависит от величины, обратной температуре, линейно. [16]
При распределении растворенного вещества между двумя несмешивающимися жидкостями возможно, что степень диссоциации распределяющегося вещества в обоих растворителях разная. Обозначим степень диссоциации его в первом растворителе ш, а во втором аз. [17]
Следовательно, распределение индивидуальных растворенных веществ смеси после п переносов можно рассчитать, если известны коэффициенты распределения веществ ( К) и объемы верхней и нижней фазы ( Ув и VH) в каждой трубке. [18]
Из закона распределения растворенного вещества между двумя несмешивающимися жидкими фазами следует, что при применении определенного количества растворителя нужно проводить извлечение не сразу всем имеющимся объемом, а несколько раз небольшими частями растворителя. [19]
Осмотические давление выравнивает распределение растворенного вещества по всему объему раствора. Электрические силы, действующие между ионами, нарушают равномерное распределение ионов в растворе. [20]
Метод анализа требует распределения растворенного вещества между хлороформом и 4 % - ным водным раствором бикарбоната натрия; в водный слой переходит только аспирин. Анализ на фенацетин и кофеин проводят одновременно из хлороформного слоя. Раствор аспирина подкисляют, экстрагируют снова хлороформом и определяют спектрофотометрически. [21]
С - коэффициент распределения растворенного вещества между жидкой и газовой фазами, / жидк - доля объема колонки, занимаемая жидкостью, Fraa - Доля объема колонки, занимаемая газом, df - толщина пленки жидкости, ОЖИКК - коэффициент диффузии растворенного вещества в жидкой фазе и и - скорость потока газа-носителя. Для пористого твердого носителя, который обычно и применяют в газовой хроматографии, толщина пленки жидкости пропорциональна отношению жидкость - твердый носитель набивки, и поэтому эффективность колонки, определяемая высотой, эквивалентной одной теоретической тарелке, должна уменьшаться с увеличением количества жидкой фазы. [22]
Основана на явлении распределения растворенных веществ между двумя не смешивающимися друг с другом растворителями. Если смешать водный раствор брома ( Вг2) и хлороформ СНСЬ, то, так как в хлороформе бром растворяется лучше, чем в - воде, он будет переходить в слой хлороформа, который приобретет вследствие этого интенсивную оранжевую окраску. Наоборот, водный раствор станет значительно бледнее, чем раньше. В конце концов установится состояние равновесия, при котором отношение концентраций брома в органическом растворителе ( С0) и в воде ( Св) станет равно некоторой постоянной величине D, называемой коэффициентом распределения. [23]
 |
Коэффициенты распределения некоторых веществ в двухкомпонентных системах несмешивающихся жидкостей при 25 С.| Схема действия ионообменного устройства для умягчения воды. [24] |
Остановимся также на распределении растворенного вещества между жидкой и твердой фазами, с которым приходится сталкиваться при изучении так называемого ионного обмена. Для осуществления этого процесса применяются специальные твердые вещества с очень большим молекулярным весом, нерастворимые в предполагаемых растворителях. На поверхности такого твердого вещества более или менее равномерно распределены электрические центры. Эти центры удерживают около себя простые ионы с зарядами противоположного знака, так что весь агломерат в целом оказывается электрически нейтральным. Простые ионы могут замещаться на поверхности твердого вещества другими ионами или, как говорят, обмениваться с ними. [25]
Экстракция основана на распределении растворенного вещества между двумя несмешивающимися фазами. [26]
Показано, что коэффициент распределения растворенных веществ остается неизменным до некоторой пороговой концентрации поверхностно-активного вещества, а затем увеличивается пропорционально концентрации. Для маноксола ОТ пороговая концентрация составляет 1 5 %, и такая, низкая концентрация этого соединения, как 0 1 %, уже обеспечивает хорошую симметрию пика. Приведенный факт может оказаться весьма полезным, поскольку Тенни [98] показал, что такие неполярные жидкости, как силикон 703, конвойл-20 и конвахлор-12, более эффективны для хроматографи-ческого разделения спиртов, чем кислородсодержащие растворители. [27]
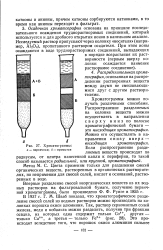 |
Хроматограммы. а-первичная. б - промытая. [28] |
Распределительная хроматография основанная на распределении растворенных веществ между двумя не смешивающимися друг с другом растворителями. [29]
Критерий подобия Ф3 характеризует коэффициент распределения растворенного вещества между двумя фазами. [30]
Страницы: 1 2 3 4