Рассмотрение - кинетическое уравнение
Cтраница 1
Рассмотрение кинетических уравнений, отражающих влияние отклонений от идеального поверхностного слоя, показывает, что они существенно отличаются от уравнений идеальной кинетики, но в ряде случаев могут совпадать с ними по форме. Поэтому формальное соответствие кинетических уравнений в обоих случаях никак не может говорить о выполнении закономерностей идеальной адсорбции. Вместе с тем существенно, что постоянные кинетических уравнений, особенно входящие в их знаменатель, имеют гораздо более сложную природу, чем предполагавшаяся ранее на основе представлений Лэнгмюра-Гиншельвуда, трактовавших эти постоянные как коэффициенты адсорбции. [1]
Рассмотрением кинетических уравнений, порядка реакций и других связанных с этим вопросов занимается формальная кинетика. [2]
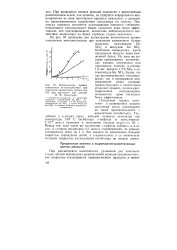 |
Кинетические кривые накопления метилэтилкетона при окислении сжиженного бутана при 135 под давлением ( по данным Н. М. Эмануэля. [3] |
При рассмотрении кинетических уравнений для начально); стадии цепной вырожденно-разветвленнои реакции предполагалось. [4]
Этот результат непосредственно следует из рассмотрения кинетического уравнения реакции. [5]
Авторы стремились также по возможности четко разграничить рассмотрение кинетических уравнений и уравнений кинетических кривых. Кроме того, в случае полного экспериментального описания процесса ( измерения всех независимых концентраций и скоростей) эти уравнения линейны относительно кинетических параметров что облегчает их определение. [6]
Физический смысл полученного решения становится нагляднее при рассмотрении кинетических уравнений, описывающих увеличение или уменьшение числа частиц определенного типа. [7]
Последнее и весьма существенное доказательство в пользу того, что мономер может прививаться, минуя стадию сорбции на полимере и непосредственно хемосорбируясь на свободных радикалах, следует из рассмотрения кинетических уравнений. Можно показать, что при наличии стадии сорбции в условиях наших опытов скорость реакции описывается уравнением, в которое концентрация свободных радикалов входит в знаменатель, что противоречит опытным данным. [8]
В последующих сообщениях мы покажем, что анализ уравнений ( 1), ( 4) и ( 5) позволяет сделать еще ряд выводов, которые не могли быть получены из рассмотрения менее точных кинетических уравнений, применявшихся ранее. В частности, нами будут даны экспериментальные зависимости величин ос и [ 5 от степени разведения спирта водой. [9]
Рассматривая в этом и предыдущих параграфах количественную трактовку закономерностей равновесия и кинетики адсорбционных процессов на неоднородных поверхностях, мы ограничились случаями, наиболее часто встречающимися на опыте, которые будут в дальнейшем использованы при рассмотрении кинетических уравнений каталитических реакций. [10]
Поэтому анализ кинетических зависимостей позволяет исключить одни варианты механизма и сделать предположения о наиболее вероятных вариантах. Рассмотрение кинетических уравнений позволяет также в некоторых случаях вынести суждение о правильности их интерпретации. [11]
Однако следует все-таки учитывать, что для сложных процессов изменение концентраций, необходимое для обращения процесса, в принципе могло бы привести и к изменению последовательности стадий. При рассмотрении кинетических уравнений процессов с учетом влияния обратной реакции принимается вытекающее из принципа микроскопической обратимости условие аналогичной последовательности стадий в прямом и обратном направлениях. [12]
Изложение неравновесной теории автор начинает с интуитивного описания ( гл. И), затем переходит к рассмотрению кинетических уравнений, их собственных значений и вычислению коэффициентов переноса ( гл. Подробно рассматривается динамика и субдинамика различных систем ( гл. Далее автор, используя диаграммный метод, переходит от общего формализма к конкретным случаям ( гл. В конце книги помещено приложение, которое является блестяще написанным очерком развития эргодической теории. [13]
Уравнение (1.14) чаще всего применяется для обобщения экспериментальных данных по кинетике массовой кристаллизации. В более общем случае анализ нестационарного процесса образования дисперсных систем может быть выполен на основании рассмотрения кинетического уравнения (1.11) при соответствующем задании начальных и граничных условий. [14]
Страницы: 1