Рассмотрим - закономерность
Cтраница 2
Рассмотрим закономерности электрохимических процессов, при протекании которых нарушается электродное равновесие в результате медленного перехода заряженных частиц через границу между электродом и раствором. В то время как стадии подвода и отвода реагирующих веществ не относятся к специфически электрохимическим стадиям, поскольку они характерны для любого гетерогенного процесса, переход заряженных частиц ( электронов или ионов) через границу раздела фаз представляет собой чисто электрохимическое явление. [16]
Рассмотрим закономерности электрохимических процессов, при протекании которых нарушается электродное равновесие в результате медленного перехода заряженных частиц через границу между электродом и раствором. [17]
Рассмотрим закономерности электрохимических процессов, при протекании которых нарушается электродное равновесие в результате медленного перехода заряженных частиц через границу между электродом и раствором. В то время как стадии подвода и отвода реагирующих веществ не относятся к специфически электрохимическим стадиям, поскольку они характерны для любого гетерогенного процесса, переход заряженных частиц ( электронов или ионов) через границу раздела фаз представляет собой чисто электрохимическое явление. [18]
Рассмотрим закономерности превращений алкилфенолов в присутствии алюмокобальтмолибденового катализатора, который является типичным гидрогенизационным катализатором, обладающим умеренной гидрирующей и крекирующей активностью. Структура этого окисного катализатора подробно не исследована, но методом рентгеноструктурного анализа и электронной микроскопии установлено, что алюминий, кобальт и молибден находятся в его составе в виде катионов. Следовательно, окислы могут играть роль Льюисовских центров, а ароматические соединения, как уже отмечалось ( см.стр. 30) будут проявлять донорный характер по отношению к этому катализатору. Проведенный нами квантово-химический расчет взаимодействия бензола, толуола и фенола с ионами алюминия и кобальта показывает, что при хемосорбции имеет место перенос заряда от ароматического кольца соединения к катиону. Это дает основание называть образующуюся на поверхности катализатора систему ароматическое соединение - катион металла я-комплексом. Отметим одновременно, что для адсорбции на металлическом никеле, как показывает расчет, должен иметь место частичный перенос электрона от атомов металла к ароматическому кольцу. Распределение этого избыточного заряда происходит по разрыхляющей орбитали ароматического соединения, что ослабляет связи в его молекуле. Следовательно, в случае восстановленного никелевого катализатора взаимодействие его с молекулой ароматического соединения аналогично по характеру нуклеофильной атаке, и можно полагать, что оно приведет к изменению закономерностей превращений алкилфенолов по сравнению с алюмокобальтмолибденовым катализатором. Это предположение находится в соответствии с экспериментальными данными. [19]
Рассмотрим закономерности движения материала в реторте без насадок, считая, что в нем находится лишь одна исследуемая нами частица. [20]
Рассмотрим закономерности электрохимических процессов, при протекании которых нарушается электродное равновесие в результате медленного перехода заряженных частиц через границу между электродом и раствором. В то время как стадии подвода и отвода реагирующих веществ не относятся к специфически электрохимическим стадиям, поскольку они характерны для любого гетерогенного процесса, переход заряженных частиц ( электронов или ионов) через границу раздела фаз представляет собой чисто электрохимическое явление. [21]
Рассмотрим закономерности протекания химической реакции, для которой выполнены оба указанных выше условия, в адиабатических условиях при фиксированном объеме. [22]
Рассмотрим закономерности процесса испарения смесей, состоящих из двух взаимно-нерастворимых и химически друг с другом не взаимодействующих жидкостей. [23]
 |
Зависимость электрохимической стандартной свободной энергии 0 от пути реакции. [24] |
Рассмотрим закономерности многоэлектронных электрохимических процессов, при которых возможен последовательный перенос электронов. [25]
 |
Зависимость скоростей выделения водорода j j и растворения ме талла ( 2 от потенциала при н (. [26] |
Рассмотрим закономерности сопряженных электрохимических реакций более подробно на примере растворения амальгам щелочных и щелочноземельных металлов. [27]
Рассмотрим закономерности движения растущего кристалла, свободно падающего в неподвижном растворе. [28]
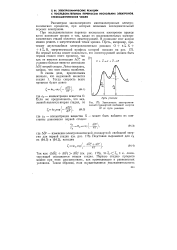 |
Зависимость электрохимической стандартной свободной энергии 0 от пути реакции. [29] |
Рассмотрим закономерности многоэлектронных электрохимических процессов, при которых возможен последовательный перенос электронов. [30]
Страницы: 1 2 3 4 5