Раствор - кислород
Cтраница 2
Выбрано, что температура жидких окиси фтора, растворов кислорода во фторе, пента-фторида хлора, диборана, водорода и метана равна нормальной температуре кипения, при которой давление насыщенного пара равно 1 атм, а температура несимметричного ди-мстилгидразина, гидразина и керосина равна 25 С. Выбрано, как это обычно делается, что энтальпии элементов в стандартном состоянии при температуре 25 С равны нулю. [16]
В [302] приведены следующие результаты по вытеснению из раствора кислорода аргоном. [17]
Скорость коррозии при наличии сероводорода усиливается присутствием в растворе кислорода. [18]
Предположение о существовании двух гидратов указанного состава в растворе кислорода в воде было сделано авторами работы [429] на основе результатов спектрофотометрического измерения коэффициентов адсорбции света растворами кислорода в воде. Приводимые данные по энтальпии образования гидратов рассчитаны из результатов измерения коэффициентов адсорбции и данных по растворимости кислорода в вюде при различных температурах. Какие-либо другие данные, подтверждающие или опровергающие существование гидратов кислорода, в настоящее время неизвестны. [19]
Скорость коррозии при наличии сероводорода усиливается присутствием в растворе кислорода. [20]
Указанный процесс может протекать только при наличии в растворе кислорода. Поскольку при работе элемента кислород расходуется, работа элемента и, следовательно, коррозионный процесс возможны только в том случае, если количество кислорода, поступающего в растрор, равно количеству расходуемого кислорода. [21]
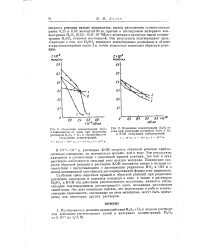 |
Изменение концентрации.| Изменение концентрации. [22] |
Глубокая связь кинетики прямой и обратной реакций при радиолизе растворов кислорода и перекиси водорода в воде, а также в растворах H2S04 и КОН под действием рентгеновского излучения, является убедительным подтверждением рассмотренного здесь механизма разложения самой воды. Это дает основание считать, что полученные в работе количественные зависимости, основанные на этом механизме, могут быть применимы для некоторых других растворов. [23]
В расплавленном состоянии наблюдается широкая область несмешивающихся жидкостей - расплава раствора кислорода в железе Ж ] и расплава окислов Жг. Температура плавления вюстита и превращения его в Жг повышается с 1371 до 1424 С по мере увеличения содержания в нем кислорода. [25]
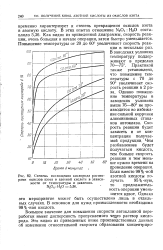 |
Степень поглощения кислорода растворами окислов азота в азотной кислоте в зависимости от температуры и давления. N2O4. Н2О 5 36. [26] |
Большое значение для повышения скорости автоклавной переработки имеет дисперсность пропускаемого черкез раствор кислорода. [27]
Измерения катодной поляризации в атмосфере водорода показали, что удаление из раствора кислорода не меняет величины катодной поляризации. Следовательно, кислород не оказывает существенного воздействия на состояние активной поверхности электрода. [28]
Газовая фаза Н2О - Н2) равновесная при 1873 К с раствором кислорода в железе ( объемное содержание кислорода 0 1200 %), содержит 72, 1 % На. [29]
Газовая фаза Н2О - Ня, равновесная при 1873 К с раствором кислорода в железе ( объемная доля кислорода 0 1200 %), содержит 72 1 % Hj. [30]
Страницы: 1 2 3 4
