Раствор - марганцовая кислота
Cтраница 1
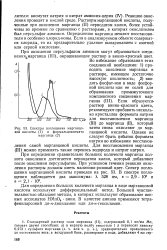 |
Спектры поглощения марганцовой кислоты ( / и формальдоксимата марганца ( 2. [1] |
Растворы марганцовой кислоты, полученные при окислении марганца ( II) периодатом калия, более устойчивы во времени по сравнению с растворами, в которых окислителем был персульфат аммония. Определению марганца мешают восстановители и особенно хлорид-ионы. Если в анализируемом объекте содержатся хлориды, то их предварительно удаляют выпариванием с азотной или серной кислотами. [2]
При окислении периодатом растворы марганцовой кислоты получаются более устойчивыми, чем при окислении персульфатом. Образующееся соединение марганцовой кислоты малиново-розового цвета имеет максимум поглощения при Я 525 нм, к 2300; определяемое минимальное количество марганца 0 01 мг в 50 мл раствора. Закон поглощения соблюдается до концентрации 150 мг / л марганцовой кислоты. [3]
При окислении периодатом растворы марганцовой кислоты получаются более устойчивыми, чем при окислении персульфатом. Добавление фосфорной кислоты в данном случае необходимо как в присутствии железа ( для связывания его в комплекс), так и в его отсутствие, так как она предотвращает возможность осаждения периодата или иодата марганца. [4]
Надсерная кислота, аналогичная надугольяой кислоте, не обесцвечивает раствора марганцовой кислоты. [5]
Надсерная кислота, аналогичная надуголь ой кислоте, не обесцвечивает раствора марганцовой кислоты. [6]
Перманганат калия хорошо растворяется в воде; раствор окрашен, как и раствор марганцовой кислоты, в интенсивный малиновый цвет. [7]
Кислотность раствора должна составлять 4 - 5 об. % по серной или 5 - - 6 об. % по фосфорной кислоте. Растворы марганцовой кислоты имеют максимум светопоглощения при 525 - 530 нм. [8]
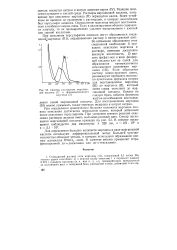 |
Спектры поглощения марганцовой кислоты ( / и формальдоксимата марганца ( 2. [9] |
Реакцию окисления проводят в кислой среде. Растворы марганцовой кислоты, полученные при окислении марганца ( II) периодатом калия, более устойчивы во времени по сравнению с растворами, в которых окислителем был персульфат аммония. Определению марганца мешают восстановители и особенно хлорид-ионы. Если в анализируемом объекте содержатся хлориды, то их предварительно удаляют выпариванием с азотной или серной кислотами. [10]
Кислотность раствора должна составлять 4 - 5 об. % по серной или 5 - 6 об. % по фосфорной кислоте. Растворы марганцовой кислоты имеют максимум светопоглощения при 525 - 530 нм. [11]
Кислотность раствора должна составлять 4 - 5 об. % по серной или 5 - 6 об. % по фосфорной кислоте. Растворы марганцовой кислоты имеют максимум светопоглощения при 525 - 530 нм. [12]
К раствору марганцовой кислоты прибавляют в избытке титрованный раствор щавелевой кислоты и нагревают до 70 С. Если это не произошло, добавляют еще щавелевой кислоты. Избыток щавелевой кислоты титруют перманганатом. [13]
К раствору марганцовой кислоты прибавляют в избытке титрованный раствор щавелевой кислоты и нагревают до 70 С. Если это не произошло, добавляют еще щавелевой кислоты. Избыток щавелевой кислоты титруют перман-ганатом. [14]
Полученную марганцовую кислоту можно прямо титровать раствором соли железа ( II) до исчезновения розовой окраски. Если в анализируемом растворе имеются другие окрашенные ионы или раствор марганцовой кислоты получился сильно разбавленным, то лучше пользоваться индикатором. При титровании разбавленных растворов рекомендуется о-фенантролин-железо ( II): 1 каплю 0 025 М раствора индикатора прибавляют на 100 мл титруемого раствора. [15]
Страницы: 1 2