Раствор - комплексонат
Cтраница 1
Растворы комплексонатов MgY2 - и ZnY2 -, а также часто употребляемых CuY2 - и HgY2 - ( как и комплексонатов других металлов) можно приготовить следующим образом. Готовят приблизительно 0 1 М растворы ЭДТА и какой-либо соли требуемого металла. [1]
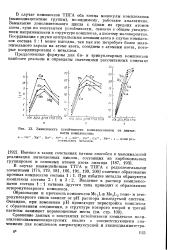 |
Зависимость устойчивости комплексонатов от дентат-ности комплексона. [2] |
Введение в раствор комплексонатов состава 1: 1 катиона другого типа приводит к образованию гетеронуклеарного комплекса. [3]
На основании исследования ИК-спектров растворов комплексонатов этилендиаминтетрауксуснои кислоты в - & с рядом металлов установлено, что способность к вытеснению бетаиновых протонов из этилендиаминтетрауксуснои кислоты уменьшается в ряду: переходные металлы редкоземельные металлы - гидролизующиеся металлыщелочноземельные металлы. [4]
При существующих в настоящее время совершенных спектрофотометрах анализу этим методом подвергаются не только окрашенные растворы. Теперь часто проводятся колориметрические определения в бесцветных растворах в ультрафиолетовой части спектра. Растворы бесцветных комплексонатов характеризуются поглощением света с короткой длиной волны. [5]
Аналогичный эффект вызывает добавление маннита к борат-ионам. В некоторых случаях оказывается полезным добавление к раствору комплексонатов металлов, образующих с сопряженным основанием смешанные комплексонаты и не создающих опасности выпадения осадков гидроксидов. [6]
Полученные продукты малорастворимы в воде, легко окисляются на воздухе и сравнительно устойчивы только в отсутствие влаги. Растворением свежеприготовленной гидроокиси железа Fe ( OH) 3 в кипящем растворе ЭДТА получен комплекс железа ( / / /) H ( FeY) - 0 4Н20 в виде крупных желто-коричневых кристаллов. Катионы алюминия, галлия, индия и таллия способны образовывать с этилендиаминтетрауксусной кислотой кристаллические комплексонаты типа HMeY - H20, которые осаждаются при введении ацетона или спирта в сильноподкисленные хлорной кислотой растворы комплексонатов. [7]
Полученные продукты малорастворимы в воде, легко окисляются на воздухе и сравнительно устойчивы только в отсутствие влаги. Растворением свежеприготовленной гидроокиси железа Fe ( OH) 3 в кипящем растворе ЭДТА получен комплекс железа ( / / /) H ( FeY) - 0 4H20 в виде крупных желто-коричневых кристаллов. Катионы алюминия, галлия, индия и таллия способны образовывать с этилендиаминтетрауксусной кислотой кристаллические комплексонаты типа HMeY - H20, которые осаждаются при введении ацетона или спирта в сильноподкисленные хлорной кислотой растворы комплексонатов. [8]
Расщепление обнаружено при исследовании растворов комплексных соединений с ионами окси - и аминополи-уксусных кислот. Таким образом, величина расщепления энергетических уровней 4f - оболочки ионов РЗЭ ( n - 100 см -) значительно меньше, чем для d - оболочки ( п - 10000 см-1), что связано с экранирующим действием внешних 5s25pe электронов. Изучение расщепления полос в спектрах поглощения растворов комплексонатов лантанидов позволяет получить некоторые сведения о симметрии внутренней сферы комплекса. [9]
Для более наглядного сравнения относительной термической устойчивости ЭДТАцетатов на рис. 4 совмещены результаты расчетов, выполненных для условий в для ряда ЭДТАцетатов. Из кривых рис. 4 видно, что термически наиболее устойчивы ЭДТАцетаты магния и кальция. Практически они не разлагаются при всех рассмотренных нами условиях. Большое значение для всего хода термолиза в парогенераторах, несомненно, имеет контакт растворов с металлом ( сталью) и одновременно присутствие в растворе комплексонатов разных металлов. Однако необходимость иметь представление о поведении раствора каждого из ЭДТАцетатов при термолизе в отсутствие контакта с металлом нам представляется первой и обязательной ступенью для изучения последующих, более сложных процессов, встречающихся на практике. [10]
Извлечение и очистка металлов в последнее время все чаще осуществляется с использованием процессов экстракции, достоинствами которых являются высокая избирательность и возможность работы как с макро -, так и микроконцентрациями. Висмут в растворах минеральных кислот ( азотной, серной, соляной, бромоводород-ной, иодоводородной) образует комплексы с анионами кислоты, причем прочность их растет от нитратных к иодидным. Он образует также сравнительно прочные комплексы с роданид-ионами и тиомочевиной. В разбавленных растворах минеральных кислот ( рН 0 4 - 2) висмут легко гидролизуется с образованием основных солей, что препятствует его экстракционному извлечению. Вследствие этого для извлечения висмута интерес представляют экстрагенты, позволяющие количественно его экстрагировать из относительно кислых сред. Гидролиз висмута предотвращают обычно введением в раствор комплексонатов, поэтому перспективны также экстрагенты, способные эффективно извлекать висмут из данных растворов. [11]
Страницы: 1