Раствор - разная концентрация
Cтраница 3
Задачи работы: измерить относительную вязкость растворов ВМВ разных концентраций; графически определить характеристическую вязкость; рассчитать молекулярную массу ВМВ. [31]
Для построения графика желательно приготовить серию растворов разной концентрации исследуемого эфира в воде, несмотря на малую растворимость этих соединений. [32]
При работе с 4 - 5 растворами разной концентрации слабого электролита строится график зависимости удельной и эквивалентной электропроводности от концентрации и разбавления. [33]
Сначала определим молярную концентрацию воды в растворах разной концентрации, затем по графику найдем парциальное давление водяных паров в этих растворах. После этого находим равновесные концентрации водяных паров в газе делением парциальных давлений воды на общее давление. [34]
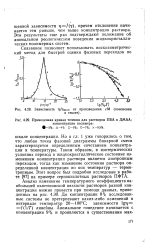 |
Зависимость т / т тах от произведения сМ ( пояснения.| Приведенная кривая течения для растворов ПБА в ДМАА. концентрация полимера. [35] |
Анализ изменения температурного коэффициента наибольшей ньютоновской вязкости растворов разной концентрации можно провести при помощи данных, приведенных на рис. 4.30. До концентрации 8 % исследованные системы не претерпевают каких-либо изменений в интервале температур 20 - 100 С; зависимости 1 § л f ( / T) линейны. [36]
Эти методы анализа основаны на сравнении окраски растворов разных концентраций. [37]
Это позволяет определить ККМ по измерениям рН растворов разной концентрации. Зависимость выражается нисходящей кривой, резко изменяющей наклон в области ККМ. Интерполируя обе части кривой, находят точку их пересечения, которую и принимают за величину lg ККМ. [38]
Для определения М нужно измерить осмотическое давление растворов разной концентрации. [39]
Затем в пробирки вносят по 1 см3 раствора тирозийа разной концентрации и добавляют в них при постоянном помешивании по 5 см3 0 5 М раствора карбоната натрия и 1 см3 рабочего раствора Фолина. [40]
Состоит из двух одинаковых электродов, погруженных в растворы разной концентрации. В нем электрический ток возникает за счет работы перенесения электролита из одного раствора в другой с иной концентрацией. Разновидностью их являются элементы, оба электрода которых образованы из растворов разной концентрации ( например, амальгамные или газовые электроды) и погружены в один и тот же раствор электролита. [41]
Колориметрический метод анализа основан на сравнении интенсивности окрасок растворов разных концентраций. Быстрота определения, возможность открытия одного иона в присутствии других без предварительного отделения обеспечили широкое распространение этого метода. [42]
Колориметрический метод основан на визуальном сравнении интенсивностей окрасок растворов разных концентраций при помощи несложных приборов: колориметрических пробирок, цилиндров с кранами, колориметров и фотометров. В колориметрии не требуется соблюдение закона Бера. [43]
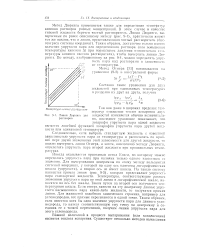 |
Линии Дюринга для растворов. [44] |
Метод Дюринга применяется также для определения температур кипения растворов разных концентраций. В этом случае в качестве типовой жидкости берется чистый растворитель. Таким образом, достаточно только одного значения упругости пара для определенного раствора ( пли повышения температуры кипения А / при нормальном давлении относительно температуры кипения чистого растворителя), чтобы вычертить линию Дюринга. [45]
Страницы: 1 2 3 4