Раствор - различная концентрация
Cтраница 1
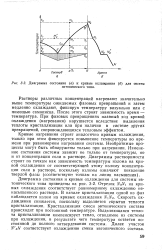 |
Диаграмма состояния ( а и кривые охлаждения ( б для систем. [1] |
Растворы различных концентраций нагревают значительно выше температуры ожидаемых фазовых превращений и затем медленно охлаждают, фиксируя температуру визуально или с помощью самописца. После этого строят зависимость время - температура. При фазовых превращениях плавный ход кривой охлаждения ( нагревания) нарушается вследствие выделения теплоты кристаллизации или при наличии в системе других превращений, сопровождающихся тепловым эффектом. [2]
Растворы различной концентрации изучены при трех температурах. [3]
Растворы различной концентрации подаются отдельными насосами и хранятся в отдельных баках. Насыщенный раствор многосернистого аммония из конечного бака подают в сборник, откуда раствор стекает в кипятильник для разложения. [4]
Растворы различной концентрации нефти поглощают разное количество света. Поэтому для каждого раствора существует его собственная оптическая плотность. Она характеризует как бы содержание в растворе особого светопоглощающего компонента. [5]
Существуют растворы различной концентрации ( см. гл. [6]
Если растворы различных концентраций разделены полупроницаемой перегородкой, через которую могут проходить молекулы растворителя, но не проходят молекулы растворенного вещества, то происходит переход молекул растворителя из менее концентрированного раствора в более концентрированный раствор. В результате этого концентрации обоих растворов постепенно выравниваются. Это явление называется осмосом. Через полупроницаемые перегородки могут проходить частицы определенного размера, обладающие определенными свойствами. [7]
Плотности растворов ТКФ различной концентрации были определены при температурах 20 и 30 С. [8]
Удельные веса растворов различной концентрации определяют циальным таблицам. [9]
При смешивании растворов различных концентраций нормальность раствора определяется общим числом грамм-эквивалентов в 1 л раствора. [10]
При смешивании растворов различных концентраций нормальность раствора определяется общим числом грамм-эквивалентов в 1 л раствора. [11]
При смешении растворов различных концентраций нормальность раствора определяется общим числом грамм-эквивалентов в 1 л раствора. [12]
Если два раствора различной концентрации разделены анионо-обмеиной мембраной, то и в этом случае возникает мембранный потенциал. Уравнение для него может быть получено аналогичным образом, только нужно учесть, что переносятся не положительно, а отрицательно заряженные частицы. [13]
 |
Схема устройства осмометра. / - раствор с. 2 - раствор ся. 3 - полупроницаемая перегородка. [14] |
При смешивании растворов различной концентрации происходит выравнивание концентрации в процессе диффузии по всему объему. [15]
Страницы: 1 2 3 4 5