Раствор - известная концентрация
Cтраница 2
Сухой адсорбент вводится далее в раствор известной концентрации и начинается процесс адсорбции. [16]
Для построения калибровочного графика используют растворы известных концентраций H2S и ММ ( 0 005 - 0 05 мг / л); ММ определяют по разности. Если концентрация ММ в анализируемой пробе превышает 0 04 мг / л, раствор разбавляют. [17]
Следовательно, измерив температуру замерзания раствора известной концентрации, можно определить молекулярную массу растворенного вещества или же концентрацию раствора. Этот метод определения широко применяется в физической химии и получил название криоскопического или метода криоскопии. Обычно при проведении криоскопических определений берут не 1000 г растворителя, а меньшее его количество - G г. Точно определяют температуру замерзания растворителя. Затем вносят в него определенное количество вещества ( т), растворяют его и измеряют температуру замерзания полученного раствора. [18]
Следовательно, измерив температуру замерзания раствора известной концентрации, можно определить молекулярную массу растворенного вещества или же концентрацию раствора. Этот метод определения широко применяется в физической химии и получил название криоскопического или метода криоскопии. Обычно при проведении криоскопических определений берут не 1000 г растворителя, а меньшее его количество - G г. Точно определяют температуру замерзания растворителя. Затем вносят в него определенное количество вещества ( / и), растворяют его и измеряют температуру замерзания полученного раствора. [19]
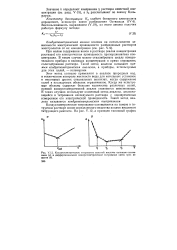 |
Кондуктометрическое титрование сильной кислоты сильным основанием ( а и дифференциальное Кондуктометрическое титрование смеси трех веществ ( б. [20] |
Значение К определяют измерением v раствора известной концентрации ( см. разд. V-15), а Я 0 рассчитывают по закону Коль-рауша. [21]
 |
Определение критической концентрации ми. [22] |
Проводят измерения сопротивления R серии растворов известных концентраций. График представляет собой две прямые линии, расположенные под тупым углом друг к другу. Из точки пересечения прямых опускают перпендикуляр на ось концентраций ( ось абсцисс) и находят величину К. [23]
Следовательно, измерив температуру замерзания раствора известной концентрации, можно определить молекулярный вес растворенного вещества или же концентрацию раствора. Этот метод определения широко применяется в физической химии и получил название криоскопического, или метода криоскопии. [24]
Определив величину предельного тока для раствора известной концентрации, можно по уравнению (4.7) определить значение множителя ( коэффициента), переводящего концентрацию в силу тока. [25]
Для титрования в объемном анализе применяют растворы известной концентрации. В этом случае концентрацию растворов выражают в единицах нормальности и титром. Нормальность раствора N - это число грамм-эквивалентов вещества, находящееся в 1 л раствора. [26]
Если эти условия стандартизировать, добавляя раствор известной концентрации в определенном количестве к определенному объему исходного раствора, то изменение рН будет зависеть от природы и концентрации исходного раствора. [27]
 |
Криоскопические постоянные некоторых растворителей. [28] |
Таким образом, измеряя температуру замерзания раствора известной концентрации, можно определить молекулярный вес растворенного вещества. [29]
Для этого достаточно измерить осмотическое давление раствора известной концентрации. [30]
Страницы: 1 2 3 4