Раствор - химическое меднение
Cтраница 2
Главным недостатком растворов химического меднения является их невысокая стабильность. В процессе меднения ( особенно в растворе, загрязненном механическими примесями) восстановление меди может происходить не только на активированной поверхности диэлектрика, но и в объеме раствора. Выделившаяся в объеме раствора медь, становясь новым центром кристаллизации, приводит к быстрому его разложению и преждевременному выходу из строя. Значительное влияние на работоспособность трилоновых растворов меднения оказывает накапливающийся в них формиат натрия. При достижении концентрации 40 г / л HCOONa раствор изменяет окраску, мутнеет и разлагается. [16]
Сравнение свойств растворов химического меднения и никелирования показывает, что раствор никелирования работает в довольно широком диапазоне рН, причем величину рН можно легко регулировать. Наоборот, раствор меднения работает в узком диапазоне рН, причем величину рН регулировать трудно. [17]
Практическое применение растворов химического меднения часто осложняется их неустойчивостью. Поэтому приходится решать задачи, связанные со стабилизацией растворов, а иногда и регенерацией отработанной ванны. [18]
Учитывая, что раствор химического меднения не допускает никаких загрязнений посторонними веществами и процесс происходит в агрессивной среде, передача ультразвуковых колебаний в жидкость осуществлена при этом через дно сосуда, установленного над вибратором. [19]
Опубликовано много рецептов растворов химического меднения с формальдегидом в качестве восстановителя. [20]
Следовательно, в растворах химического меднения формальдегид присутствует главным образом в виде метилен-гликоля и его аниона. [21]
Следовательно, в растворах химического меднения формальдегид присутствует главным образом в виде метиленгликоля - и его аниона. [22]
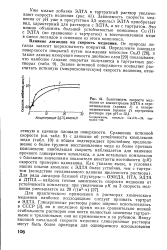 |
J. Зависимость скорости меднения от концентрации ЭДТА в перемешиваемом ( кривая 1 и неперемешиваемом ( кривая 2 тартратном 20 - - - - - - - - - - - JO Растворе при рН 12 1. [23] |
Для практического применения в растворах химического меднения наиболее подходящими следует признать тартрат и ЭДТА. Глицериновые растворы ранее широко использовались в СССР [3], но в последнее время из-за сравнительно низкой стабильности растворов они почти полностью заменены тартрат-ными и трилоновыми; они не применяются и за рубежом. [24]
Для практического применения в растворах химического меднения наиболее подходящими следует признать тартрат и ЭДТА. Глицериновые растворы ранее широко использовались в СССР, но в последнее время из-за сравнительно низкой стабильности растворов они почти полностью заменены тартратными и трилоно-выми; их не применяют и за рубежом. Ввиду высокой начальной скорости меднения глицериновые растворы могут быть более пригодны для однократного использования при меднении мелких деталей в условиях большой степени загрузки. [25]
Поэтому важное значение имеет стабилизация растворов химического меднения. [26]
Практически единственным восстановителем, используемым в растворах химического меднения, является формальдегид. Он доступен и дешев, позволяет получить медные покрытия при комнатной температуре. Си катализирует реакцию восстановления и поэтому при определенных условиях реакция идет лишь на требуемой поверхности, а в объеме раствора медь не восстанавливается. [27]
Практически единственным восстановителем, используемым в растворах химического меднения, является формальдегид. Он доступен и дешев, позволяет получить медные покрытия при комнатной температуре. [28]
Возможно, будет найден простой способ стабилизации растворов химического меднения, но в любом случае останется нерешенной проблема коррозии на границе раздела медь-никель. К тому же малая стойкость к окислению тонкой пленки меди, полученной химическим путем, и, главное, некоторые особенности процесса гальванопокрытия требуют применения подвесок и держателей двух типов. [29]
Дальнейший ход кривых позволяет предположить, что в растворе химического меднения состав, строение и константа неустойчивости комплексов зависят от рН среды. Кроме того, при концентрации NaOH более 1 0 моль / л поверхность пассивирует гидро-ксильный ион. Цвет осадка также зависит от этого фактора; при концентрации NaOH менее 0 75 моль / л осадок светло-коричневый, а при концентрации 1 0 - 2 5 моль / л - розоватый. [30]
Страницы: 1 2 3