Раствор - сернокислая медь
Cтраница 3
Наиболее простым электролитом служит раствор сернокислой меди с добавлением, для улучшения электропроводности, серной кислоты. [31]
Наиболее простым электролитом служит раствор сернокислой меди с добавлением, для улучшения электропроводности, серной кислоты. В этих электролитах медь осаждается из двувалентных ионов, электрический эквивалент ее 1 186 г / час. Кислые электролиты обладают плохой рассеивающей способностью, но устойчивы в работе и позволяют применять высокие ( до 30 а / дм2) плотности тока. Основным недостатком кислых медных ванн является то, что в них нельзя производить осаждения непосредственно на сталь и чугун. При погружении этих металлов в раствор на поверхности их выделяется контактная ( без действия тока) медь, имеющая плохое сцепление с основным металлом и обладающая большой пористостью. Поэтому изделия из железных сплавов должны быть предварительно покрыты медью в цианистой ванне или никелем толщиной 2 - 3 мк, после чего наращивание меди ведется в кислой ванне. Кислые ванны применяются также для наращивания медных изделий ( например, типографских валов) и для гальванопластики. [32]
Фелингова жидкость - смесь растворов сернокислой меди, сегнетовой соли ( см. стр. [33]
К фильтрату прибавляют немного раствора сернокислой меди и несколько капель концентрированного раствора аммиака. [34]
Приливают 0 5 мл раствора сернокислой меди, содержащей 10 мг Си / мл, 5 мл 10 % - ного раствора тиомочевины, раствор разбавляют водой до - 22 мл и тщательно перемешивают. Затем растворы переводят в цилиндры. [35]
При выдерживании пластинки в растворе сернокислой меди, с одной стороны, определенное количество железа переходит в раствор и, с другой стороны, на пластинке осаждается медь, количество которой может быть рассчитано по уравнению реакции. [36]
Илосвая на ацетилен; - раствор сернокислой меди, аммиака и солянокислого гидроксиламина, взятых в определенной пропорции; например, к раствору 1 г CuSO4 в 8 мл 10 % - ного аммиака добавляются 3 г солянокислого гидроксиламина и вода до объема 50 мл; в присутствии ацетилена в растворе образуется красный осадок. [37]
Какой заряд должен пройти через раствор сернокислой меди, чтобы на катоде отложилось 6 58 г меди. [38]
Какой заряд должен пройти через раствор сернокислой меди, чтобы на катоде отложилось 6 58 г медн. [39]
При внесении ингибированного образца в раствор сернокислой меди его поверхность остается некоторое время ( в отдельных случаях до нескольких часов) без изменения. Затем на образце появляются отдельные точки осажденной меди, которые очень медленно увеличиваются в размерах. Это указывает на то, что экранирующие свойства защитной пленки ингибитора на металле не везде равноценны. Постепенно места, занятые осадив-шейся медью, расширяются, захватывая все большую площадь образца, пока, наконец, защитная пленка не исчезает с поверхности металла. [40]
К 3 каплям 7 % раствора сернокислой меди прибавляют 3 капли щелочного раствора сегнетовой соли. К полученному реактиву Феллинга добавляют 5 - 6 капель исследуемой мочи, жидкость перемешивают и нагревают до начала кипения. В - присутствии глюкозы выпадает желтый осадок гидрата закиси меди или красный осадок закиси меди. [41]
Так, например, из раствора сернокислой меди выделяется пятиводный кристаллогидрат CuSO4 5Н2О, который называется медным купоросом. [42]
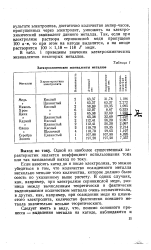 |
Электрохимические эквиваленты металлов. [43] |
Так, если при электролизе раствора сернокислой меди пропущено 100 а - %, то при этом на катоде выделится, а на аноде растворится 100 X 1 18 118 Г меди. [44]
В пробирку помещают 2 капли раствора сернокислой меди и 2 капли раствора едкого натра. К выпавшему голубому осадку гидроокиси меди ( II) добавляют раствор средней соли виннокаменной кислоты ( см. опыт 98) - сегнетовой соли. Голубой осадок растворяется и образуется раствор ярко-синего цвета, содержащий комплексный ион меди. Полученный щелочной раствор комплексного медного производного сегнетовой соли известен под названием жидкости Фелинга и обладает окислительными свойствами. [45]
Страницы: 1 2 3 4