Раствор - щелочной щелочноземельный металл
Cтраница 2
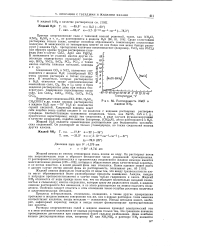
Кривые, подобные кривым аномальной электропронодпостн электролитов в невидных органических растворителях, бьи и получены при изучении растворов щелочных и щелочноземельных металлов г жидком аммиаке. Па кривой молярной электропроводности раствора натрии в жидком аммиаке ( рис. 5.6) при определенном составе раствора наблюдается мшимум проводимости, после чего она растет с разведением, приближаясь к некоторому предельному значению. [16]
Представление о возможности существования в растворах электронов как независимых частиц было выдвинуто еще в 1908 г. Крауссом [8], предположившим, что эти частицы могут присутствовать в растворах щелочных и щелочноземельных металлов в жидком аммиаке. [17]
Чистый безводный гидразин ионизирован лишь в незначительной степени. Хотя растворы щелочных и щелочноземельных металлов вполне устойчивы в жидком аммиаке, что, повидимому, связано с малой концентрацией ионов аммония в самом растворителе, однако подобные растворы не могут быть приготовлены в безводном гидразине. Растворение металлического натрия в безводном гидразине сопровождается появлением быстро исчезающей синей окраски. [18]
Эти наблюдения, казалось бы, свидетельствуют об особой роли свободно выделяющегося водорода в момент выделения, однако правильнее и в этих случаях принять иной механизм восстановления. Исследуя свойства растворов щелочных и щелочноземельных металлов в жидком аммиаке и протекающие в них реакции, Краус [27-31] пришел к выводу, что эти реакции имеют ионный характер. Краус считал, что, растворяясь в жидком аммиаке, натрий частично образует положительные ионы Na; отрицательными ионами являются свободные электроны, соль-ватированные молекулами аммиака. [19]
Класс смешанных проводников состоит из веществ, обладающих частично электронной и частично ионной проводимостью. К ним относятся, например, растворы щелочных и щелочноземельных металлов Б жидком аммиаке, некоторые жидкие сплавы и соли ( р-мо-дификация сульфида серебра, бромистая медь), характер проводимости которых меняется в определенном интервале температур, и другие вещества. [20]
Деление проводников в зависимости от типа проводимости ( электронная или ионная) является условным. Подобный же переход к смешанной проводимости наблюдается в растворах щелочных и щелочноземельных металлов в жидком аммиаке при увеличении концентрации. [21]
Металлическая ртуть извлекает калий с восстановлением структуры графита, а при действии на С8К жидкого аммиака происходит частичное замещение атомов калия молекулами МН3 по схеме: ЗС8К 4NH3 2Ci2K ( NH3) 2 К. Подобные же синие металло-аммиачные производные графита с расстояниями между паркетами около 6 6 А могут быть получены прямым его взаимодействием с растворами щелочных и щелочноземельных металлов в жидком аммиаке. Вещества эти очень чувствительны к влаге, но на воздухе не самовоспламеняются. [22]
Ионы электролитов сольватируются в жидком аммиаке почти так же, как в воде ( стр. Жидкий аммиак растворяет также и другие вещества. Представляют интерес растворы щелочных и щелочноземельных металлов в жидком аммиаке, имеющие темно-голубой цвет. В этих растворах металлы сохраняют свои химические свойства. [23]
С химической стороны СаК характеризуется исключительной реакционной спо-1 собностью. Металлическая ртуть извлекает калий с восстановлением структуры графита, а при действии на СвК жидкого аммиака происходит частичное замещение атомов калия молекулами МНз по схеме: ЗСвК-f 4МНз 2С1гК ( МНзЬ К. Подобные же синие металло-аммиачные производные графита с расстояниями между паркетами около 6 6 А могут быть получены прямым его взаимодействием с растворами щелочных и щелочноземельных металлов в жидком аммиаке. Вещества эти очень чувствительны к влаге, но на воздухе не самовоспламеняются. [24]
 |
Растворимость NaCl в жидком NH3. [25] |
Жидкий аммиак формально отличается от воды тем, что ввиду трехвалентности азота могут образовываться более разнообразные продукты замещения. Амидам, имидам и нитридам противопоставляются в случае воды только гидроокиси и окиси. Жидкий NH3 отличается от воды прежде всего тем, что он обладает значительно меньшей склонностью к сольволизу; многие соединения, которые сразу же разлагаются водой, в жидком аммиаке растворяются без изменения, и из этого растворителя их можно выделять осаждением. Особенно следует отметить в этом отношении темно-голубые растворы щелочных и щелочноземельных металлов. [26]
Страницы: 1 2