Раствор - система
Cтраница 2
Изучены [75] термодинамические свойства растворов системы Н3РО4 - H2SC4 - Н2О в интервале температур от 25 до 90 С при массовом или молярном отношении Н3РО4: H2SO4 ( Д) от 155 до 0 23 и содержании воды от 0 92 до 0 62 мол. [16]
Из растворов молибденового производства ( растворы систем пылеулавливания и маточные растворы после выделения пара-молибдатов) примерного состава, г / л: 0 01 - 0 05 Re; 2 5 Mo; 80 - 100 SO - j 50 - 100 С1, рений наиболее эффективно поглощается на сильноосновных анионитах Вофатит SBW и АВ-17. Емкость их составляет - 50 - 60 % ( по массе) по рению. [17]
Сведения о плотности и вязкости растворов системы KNO3 - HNO3 - Н2О, которые могут найти применение в производстве концентрированной азотной кислоты и сложных удобрений [12, 13], в литературе отсутствуют. [18]
Результаты определения давлений паров над растворами систем HNO3 - Н3РО4 - HF - Н2О и влияние на него добавок CaO, Fe2O3, A12O3 свидетельствуют, что введение указанных добавок приводит к повышению давления паров HNO3 и воды. Присутствие Mg также способствует повышению давления паров НЫОз и воды над раствором. [19]
При любой заданной температуре из всех возможных растворов системы ( кроме пересыщенных) давление пара эвтонического раствора является наименьшим. Поэтому кривые давления пара эвтонических растворов должны целиком располагаться внутри областей, ограниченных кривыми давления пара насыщенных растворов солей, образующих данную систему, но взятых в отдельности. [20]
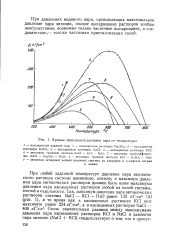 |
Кривые зависимости давления пара от температуры. [21] |
При любой заданной температуре давление пара эвтониче-ского раствора системы наинизшее; поэтому и максимум давления пара эвтонических растворов должен быть ниже максимума давления пара насыщенных растворов любой из солей системы, взятой в отдельности. [22]
Парциальные упругости НС1 - газа над растворами систем: Си2С12 - НС1 - Н2О; TiCl4 - НС1 - Н2О; ZrCl4 - HC1 - Н2О при 25, Отч. [23]
Кроме указанных факторов, на электрические свойства растворов систем 1 - 6 существенное влияние оказывает доля ионной составляющей связи в них. [24]
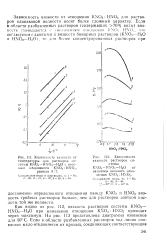 |
Зависимость вязкости от температуры для растворов системы KNO3 - HNO3 - H2O с весовым отношением KNO3. HNO3, равным 3. 7. [25] |
Как видно из рис. 112, вязкость растворов системы KNO3 - HNO3 - Н20 при изменении отношения KNO3: HNO3 проходит через максимум. На рис. 113 представлена диаграмма изовискоз для 50 С. [26]
Образование октогена в присутствии нитрата аммония в растворе системы НМО3 - ( СН3СОЬО означает, что МН4МОз либо облегчает удаление формальдегида, либо препятствует этерификации. Так, известно, что когда нитрат аммония растворяется в этрй. [27]
Обраэованиг охтогена в присутствии нитрата аммопня в растворе системы HNO - ( CHjCO) iO означает, что MI. NOj либо облегчает удаление формальдегида, либо препятствует этернфикацин. Повышенно температуры, по-видимому, необходимо для отщепления формальдегида. [28]
Данныеш о растворимости метастабильной фазы СаНРО4 2Н2О в растворах системы СаО - P2Os - H2O ( рис. 261) и о скорости полиморфного превращения СаНРО4 2Н2О - СаНРО4 при 40 ( рис. 262) подтверждают возможность образования метастабильного брушита, который превращается в стабильную безводную соль тем скорее, чем выше концентрация P2Os в жидкой фазе. Этот вопрос имеет большое значение в производстве преципитата как удобрения, потому что потеря кристаллизационной воды при фазовом превращении брушита в растворах вызывает заметное ( до 50 отн. [29]
При наложении внешнего электрического поля вдоль находящейся в растворе системы капилляров, подвижные ионы диффузного слоя, пере -, двигаются к противоположному полюсу. [30]
Страницы: 1 2 3 4 5