Раствор - соль - редкоземельный элемент
Cтраница 1
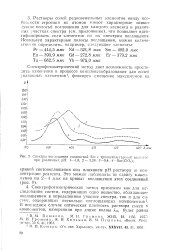 |
Спектры поглощения соединений Sm с трпоксиглутаровой кнслито. при различных рН. У - 1 8. 2 - 3 28. 5 - 9 4. 4 - Sm ( CtO4 r. [1] |
Растворы солей редкоземельных элементов ввиду особенности строения их атомов имеют характерные пики ( узкие полосы) поглощения для каждого элемента в различных участках спектра ( см. приложение), что позволяет идентифицировать соли элементов по их спектрам поглощения. [2]
Раствор соли редкоземельного элемента, содержащий 0 1 мг в 1 мл. [3]
К раствору соли редкоземельного элемента ( отдельному или смеси), помещенному в мерную колбу на 50 мл и содержащему редкоземельный элемент в количестве от 0 5 мг до 5 мкг, прибавляют 5 мл раствора арсеназо I, 0 5 мл соляной кислоты и 1 5 мл уротропина ( для создания рН 6 5) и доводят объем раствора водой до метки колбы. После перемешивания отбирают пипеткой 20 мл этого раствора и переносят в кювету для титрования. Настройку спектрофотометра производят так, как указано на стр. [4]
Спектры поглощения растворов солей редкоземельных элементов ввиду особенностей строения 4 / - оболочки состоят из определенного числа довольно узких максимумов, расположенных при определенных длинах волн. [5]
Снимают спектр поглощения раствора соли редкоземельного элемента, пользуясь спектрофотометром СФ-4 и фо-тоэлектроколориметрами ФЭК-56, ФЭК-Н-54, ФЭК-Н-57 ( или фотометром ФТ), и строят кривые полученных спектров. [6]
К тому же раствору соли редкоземельного элемента прибавляют лимонную кислоту и щелочь. [7]
Так, при разведении растворов солей редкоземельных элементов с малым количеством носителя, все стадии разведения следует проводить однонормальным раствором кислоты. [8]
Для проведения качественного анализа раствора солей редкоземельных элементов снимают спектр поглощения анализируемого раствора и определяют наличие характерных максимумов для тех или других элементов. [9]
 |
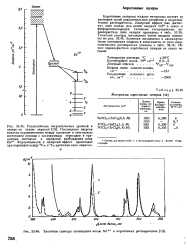
Окраска аквокатионов некоторых элементов и заполнение d - орбиталей. [10] |
Большой интерес представляют спектры поглощения растворов солей редкоземельных элементов и актинидов. Эти спектры, связанные с наличием заполняющихся / - орбиталей при занятых более высоких s - и р-подуровнях, весьма сложны и сохраняют дискретную структуру, в какой-то мере сходную со структурой спектров атомарных газов. Различия в электронной конфигурации отдельных элементов обусловливают высокую индивидуальность спектров растворов их солей. [11]
Особый интерес представляют спектры поглощения растворов солей редкоземельных элементов и актиноидов. Они имеют почти одинаковое электронное строение внешних орбиталей. Поэтому данные элементы очень похожи друг на друга по своему химическому поведению и трудно разделимы. Оптические спектры редкоземельных элементов возникают в результате возбуждения именно этих наименее прочно связанных, но достаточно экранированных электронов. Эти спектры очень сложны и резко отличаются друг от друга. [12]
Особый интерес представляют спектры поглощения растворов солей редкоземельных элементов и актиноидов. Они имеют почти одинаковое электронное строение внешних орбиталей. Поэтому данные элементы очень похожи друг на друга по своему химическому поведению и трудно разделимы. Оптические спектры редкоземельных элементов возникают в результате возбуждения именно этих наименее прочно связанных, но достаточно экранированных электронов. Эти спектры очень сложны и резко отличаются друг от друга. [13]
Из неорганических соединений собственной флюоресценцией обладают растворы солей редкоземельных элементов, соединения, содержащие положительный ион уранила, и некоторые комплексные соли металлов. [14]
Страницы: 1 2