Раствор - сульфат - титан
Cтраница 1
Раствор сульфата титана ( III) в 4 N серной кислоте более устойчив на воздухе. [1]
Раствор сульфата титана ( IV) готовят растворением TiO2 в концентриро ванной серной кислоте при нагревании. [2]
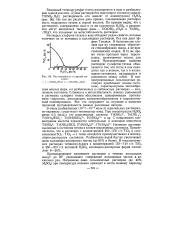 |
Растворимость в серной кислоте. [3] |
Растворы сульфатов титана в воде обладают рядом свойств, которые отличают их от истинных и коллоидных растворов. Все они дают эффект Тиндаля. В большинстве случаев при их упаривании образуется стеклообразная масса, а не кристаллический осадок. В то же время титан проходит через перегородку, проницаемую только для ионов. Противоречивые свойства растворов сульфатов титана объясняются тем, что титан в них находится как в ионном, так и в коллоидном состояниях, находящихся в равновесии между собой. В концентрированных сильнокислых растворах преобладает ионное состояние, характеризуемое многообразием ионных форм, а в разбавленных и слабокислых растворах - коллоидное состояние. Сложность и метастабильность ионных равновесий в растворах сульфата титана обусловлена одновременным протеканием гидролиза, диссоциации, комплексообразования и гидролитической полимеризации. Все это затрудняет их изучение и является причиной противоречивости данных различных авторов. [4]
Раствор сульфата титана Ш) более устойчив. [5]
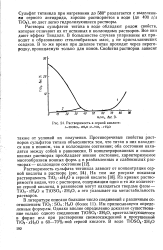 |
Растворимость в серной кислоте.. - тюзо4 2Н2о. 2 - тю2 х Н2о. [6] |
Растворы сульфатов титана в воде обладают рядом свойств, которые отличают их от истинных и коллоидных растворов. Все они дают эффект Тиндаля. В большинстве случаев упаривание их приводит к образованию стеклообразных масс, а не кристаллических осадков. В то же время при диализе титан проходит через перегородку, проницаемую только для ионов. [7]
Растворы сульфата титана для технических целей получают разложением титансодержащего сырья серной кислотой. Основным видом титансодержащего сырья являются ильменитовые концентраты, содержащие ильменит FeTiO3, продукты его лейкоксенизации ( выветривания) - FeO, Fe2O3 и ТЮ2, а также титанистые шлаки. [8]
Раствор сульфата титана ( III) является боле. [9]
Растворы сульфатов титана обладают различной степенью устойчивости, которая зависит от концентрации титана и серной кислоты. [10]
Раствор сульфата титана ( III) имеет фиолетовый цвет сохраняют его в склянке из темного стекла, защищая о1 прямого солнечного света. Для восстановления Ti ( IV 200 мл приготовленного раствора встряхивают с 300 мл жид кой амальгамы цинка в течение 1 мин и переливают в бу тыль для хранения раствора. [11]
Растворы сульфата титана гидролизуют при нагревании с выделением в осадок нерастворимого гидроксида титана. Процесс этот значительно ускоряется в присутствии так называемых зародышей. Последние представляют собой тонкодисперсную взвесь гидроксида титана в воде. Частички взвеси могут иметь как ана-тазную, так и рутильную структуру. [12]
Раствор сульфата титана, содержащий перекись водорода. Для его приготовления 0 2 г высушенной при 150 С двуокиси титана сплавляют в платиновом тигле с 4 г пиросульфа-та калия. Охлажденный сплав выщелачивают 5 % - ным ( по объему) раствором серной кислоты. Раствор переводят в мерную колбу емкостью 1 л, прибавляют около 500 мл 5 % - ной H2SO4, 6 мл 30 % - ного раствора перекиси водорода и снова 5 % - ной серной кислоты до метки. [13]
Получение растворов сульфата титана включает в себя несколько операций: разложение титансодержащего сырья; выщелачивание плава; восстановление Fe3 в Fe2; очистку раствора от шлама; выделение FeSO4 - 7H2O; концентрирование раствора. [14]
Гидролиз растворов сульфата титана проводят в стальных аппаратах, футерованных кислотоупорными плитками и снабженных освинцованными мешалками и змеевиками для нагрева и охлаждения реакционной смеси. При достижении степени гидролиза 70 - 75 % к суспензии добавляют воду в количестве 35 - 40 % по отношению к начальному объему раствора. Разбавлением снижают концентрацию кислоты в конце гидролиза и способствуют этим повышению степени гидролиза, так как высокий кислотный фактор замедляет скорость процесса. В результате гидролиза 95 - 97 % титана переходит в осадок. Серная кислота и соли Fe2 и других металлов обычно остаются в растворе. [15]
Страницы: 1 2 3 4