Раствор - углеводород
Cтраница 1
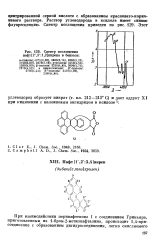 |
Спектр поглощения нафт [ 2 3. 1 2 пирена в бензоле. [1] |
Раствор углеводорода в ксилоле имеет синюю флуоресценцию. [2]
Раствор углеводорода в 1-метил-нафталине окрашен в зеленый цвет, в этом растворе он подвергается фотоокислению. [3]
Раствор углеводорода в органических растворителях окрашен в синий цвет. [4]
 |
Спектр поглощения ЗЯ-45 - бензнафтантрена в бензоле. [5] |
Раствор углеводорода в концентрированной серной кислоте окрашен в зелено-синий цвет, раствор - в бензоле обладает голубой флуоресценцией. [6]
Растворы углеводородов в четыреххлористом углероде можно анализировать методом ИК-снектрометрии по специфической для СН-группы длине волны, при которой этот растворитель не поглощает света. Для полуколичественного определения высших углеводородов может служить и их способность люминесцировать. [7]
Раствор углеводородов подвергается равновесной дистилляции под давлением 10атаво время прохождения по трубам, обогреваемым снаружи. [8]
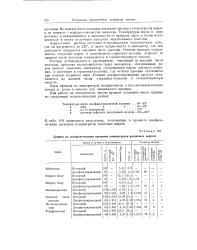 |
Данные по деасфальтизации пропаном концентратов различных нефтей. [9] |
Раствор углеводородов в растворителе, отводимый из верхней части колонны, проходит последовательно через эвапоратор, обогреваемый паром низкого давления, эвапоратор, обогреваемый паром высокого давления, и поступает в стриппинг-колонну, где остатки пропана отгоняются при помощи открытого пара. Готовый деасфальтированный продукт откачивается из нижней части стриппинг-колонны в соответствующую емкость. [10]
К раствору углеводорода в эфире добавляют пикриновую кислоту, также растворенную в эфире. Нафталин при этом образует осадок состава C10H8 - C6H2 ( NO2) 3OH, кристаллизующийся в виде желтых игл. Кристаллы, имеющие форму оранжевых игл, образуются при осаждении фенантрена, флуорена; кристаллы в виде красных игл характерны для антрацена, карбазола, пирена, хри-зена. Чтобы уменьшить скорость испарения эфира, эти реакции необходимо проводить, как указано на стр. [11]
В растворе углеводорода аналогичные реакции, по-видимому, протека ют гораздо медленнее, но при температуре окисления около 100 - 150 С и они все же могут происходить с достаточно большими скоростями. [12]
В растворе углеводорода аналогичные реакции, по-видимому, протекают гораздо медленнее, но при температуре окисления около 100 - 150 С и они все же могут происходить с достаточно большими скоростями. [13]
В растворе углеводорода аналогичные реакции, по-видимому, протекают гораздо медленнее, но при температуре окисления в 100 - 150 и они могут проходить достаточно быстро. [14]
В растворе углеводородов соли металлов находятся в недиссоциированной форме. В результате образования полярных продуктов в окисляющемся углеводороде степень ассоциации молекул соли снижается, поскольку появляются комплексы типа соль-продукт. [15]
Страницы: 1 2 3 4