Раствор - фторид
Cтраница 1
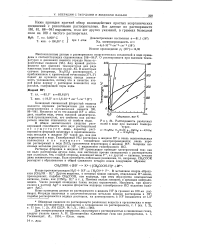 |
Растворимость различных солей в воде при высоких температурах. [1] |
Растворы фторидов в жидком HF превосходно проводят электрический ток; как ни мало растворимы другие соли, они настолько прочно связываются с растворителем при сольволизе, что, с одной стороны, возникают ионы F -, ас другой - катионы, отчасти даже неизвестного вида. [2]
Раствор фторида нейтрализуют в платиновой чашке, насыщают поваренной солью в стакане для титрования, добавляют равный обьем спирта и титруют с платиновыми электродами при пропускании СО. [3]
Осаждением растворов фторидов щелочью получаются осадки неустойчивых форм гидроксофторидов. [4]
Из растворов фторидов хлорид калия не выделяет осадка. [5]
Для растворов фторидов, сульфатов и некоторых других солей щелочных металлов одинаковой концентрации форма кривых совпадает. [6]
Реакция растворов фторидов близка к нейтральной. [7]
Изучение растворов фторидов - оснований не вызывает особого интереса, так как фтористый водород выступает здесь формально в роли акцептора фтор-иона, что для него менее характерно, нежели ионизация с отщеплением протона и присоединением Н к молекуле растворенного вещества. Последнее наблюдается при растворении в HF и органических, и неорганических веществ, причем среди неорганических веществ особый интерес представляет вода. [8]
Условия равновесия растворов фторидов, содержащих высокую концентрацию F и низкую концентрацию SiF6, были разобраны ранее. Большинство металлов образует хорошо растворимые гек-сафторосиликаты и трудно растворимые фториды. [9]
Присутствие в растворе фторидов мешает образованию фосфо-ромолибдата, поэтому если для разложения руды применялась фтористоводородная кислота, фтор связывают в комплекс HBF4, прибавлением к раствору буры или борной кислоты. [10]
При добавлении в раствор фторидов или растворимых оснований осаждаются нерастворимые трифториды или гидроокиси. Сульфиды в растворе не образуются. Редкоземельные элементы образуют в растворе большое число комплексных ионов и соединений, из них особенно прочны комплексы с клешневидными агентами. [11]
Наиболее подробно изучены растворы простых фторидов в HF. Как и большинство электроотрицательных элементов, фтор образует простые фториды со всеми элементами, за исключением гелия, неона и аргона. Фториды могут быть классифицированы в зависимости от вида ионов, которые они образуют при растворении в жидком фтористом водороде. [12]
При выполнении анализов растворов чистых фторидов, содержащих от 1 до 50 мг фтора, были получены результаты, отклоняющиеся от теоретических не больше чем на 0 1 мг. [13]
Определение основано на титровании раствора фторида никеля трилоном Б в присутствии мурексида в качестве индикатора. [14]
Интересный материал дает химия растворов фторидов ксенона в инертных растворителях. Диссоциация XeFn на XeF j и F - становится возможной в растворителях с высокой диэлектрической проницаемостью или в растворителях, где молекулы растворителя образуют связи с растворенными соединениями ( например, HF в HF) ( ср. [15]
Страницы: 1 2 3 4