Раствор - хлорат
Cтраница 2
Если к этому остатку добавить воды, то получается раствор хлората аммония NH4C1O3 реактивной квалификации. [16]
Если к этому остатку добавить воды, то получается раствор хлората аммония NH4C103 реактивной квалификации. [17]
Нитрат серебра, ацетат свинца и хлорид бария из растворов хлоратов осадков не выделяют. [18]
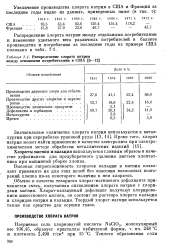 |
Распределение хлората натрия между основными потребителями в США. [19] |
Хлорат-кальциевый дефолиант получают хлорированием известкового молока, он состоит из раствора хлората кальция и хлоридов натрия и кальция. Твердый хлорат магния используется также как средство для осушки газов. [20]
На часовом стекле ( или в фарфоровой чашечке) к капле раствора хлората и иодида ( в 10 мл по 1 г каждой соли)) прибавляют каплю серной кислоты ( 1: 1000) и по 1 капле нейтрального испытуемого и крахмального растворов. В присутствии осмия появляется синее окрашивание. [21]
При электролитическом получении хлорнокислого калия ( перхлората калия) пользуются как исходным материалом растворами хлоратов. [22]
Далее хлорат калия и хлорат натрия растворяют в воде; к раствору добавляют с небольшим избытком раствор хлората нлатины ( 10 %), а затем исследуемый раствор выпаривают почти досуха и охлаждают. [23]
Затем приливают по 0 10 мл раствора пирофосфата, 2 мл раствора сернокислого анилина, 1 мл раствора хлората и 0 10 мл раствора оксина. Перемешивают и нагревают в кипящей воде 5 мин. Стандартный раствор содержит 0 5 мкг V в 1 мл. [24]
Недостатком окисно-свинцовых анодов является также образование загрязненных свинцом стоков как в основном производственном процессе, так и на стадии приготовления этих анодов, а также загрязнение раствора хлората солями свинца. [25]
Применяемая для уплотнения бетонов силикатизация может быть достигнута при помощи пропитки верхних слоев изделий из бетона или горных пород раствором жидкого стекла, а после высыхания последнего - раствором хлората или хлорида кальция. [26]
Так как одним из проявлений действия перхлоратов является сильное искривление побегов, вызывает сомнение сообщение Ямасаки14, утверждающего на основании измерения роста растений, что 0 5 % - ный раствор перхлората более токсичен, чем 1 % - ный раствор хлората. [27]
Соли хлорноватистой кислоты ( гипохлориты) и хлористой ( хлориты) в свободном состоянии неустойчивы и являются сильными окислителями в водных растворах. Растворы хлоратов и перхлоратов щелочных металлов, напротив, устойчивы, показывают нейтральную реакцию и не проявляют окислительных свойств. Хлораты и перхлората могут быть выделены в свободном состоянии. [28]
Раствор хлората пропускают через катионит, а полученную хлорноватую кислоту восстанавливают до двуокиси хлора. [29]
Соли хлорноватистой кислоты ( гипохлориты) и хлористой ( хлориты) в свободном состоянии неустойчивы и являются сильными окислителями в водных растворах. Растворы хлоратов и перхлоратов щелочных металлов, напротив, устойчивы, показывают нейтральную реакцию и не проявляют окислительных свойств. Хлораты и перхлораты могут быть выделены в свободном состоянии. [30]
Страницы: 1 2 3