Раствор - двуокись - углерод
Cтраница 2
Выделение водорода из воды по уравнению (2.19) даже в присутствии очень неблагородных металлов типа магния, алюминия и цинка сильно затруднено; в принципе оно возможно по уравнению (2.18) из кислот, например из раствора двуокиси углерода или из органических кислот, содержащихся в грунте. Однако агрессивное коррозионное действие кислот обусловливается не столько их участием в катодной частичной реакции, сколько затруднением образования защитного поверхностного слоя из продуктов коррозии. Из-за этого протекание промежуточных частичных реакций по уравнениям (2.17) и (2.21) затормаживается в меньшей степени. [16]
Вторая серия работ по фотосинтезу in vitro представлена опытом Дхара и его сотрудников; они утверждают, что положительные реакции на формальдегид получаются при выставлении на несколько часов на тропический солнечный свет открытых сосудов с растворами двуокиси углерода или карбонатов. Авторы не разъясняют, в каких отношениях этот свет отличен от солнечного света всех иных районов или от света искусственных источников. Формальдегид можно обнаружить даже в чистых растворах углекислого газа или двууглекислого натрия [127, 141, 142, 145]; выход формальдегида увеличивается при введении следующих сенсибилизаторов. Для растворов двуокиси углерода: FeCl3, Fe ( OH) 3, FeS04, NiS04, CoCOs, CuS04, CuC03, ацетат Си, Cr2 ( SOJ3, Cra08, Cr ( OH) 3, MnCl2, V205, NH4 - Се-нитрат, Pd ( N03) 2, UOa ( N08) 2, метиленовая синь, метилоранж и малахитовая зелень. [17]
Если давление уменьшить, то газ начинает выделяться из раствора в виде пузырьков. При прекращении выделения пузырьков раствор двуокиси углерода оказывается все же пересыщенным, Если помешать такой раствор палочкой, то вновь появляются пузырьки. Относительно хорошей растворимостью двуокиси углерода в воде под давлением пользуются для изготовления газированной воды. При повышении температуры растворимость двуокиси углерода уменьшается. [18]
Назовем шампанское, для которого выполняется уравнение ( 2), совершенным. Выясняется, что для раствора двуокиси углерода в воде оно будет выполняться при температуре Т 15 С. Анализируя уравнение далее, можно сделать вывод о том, что если при открывании бутылки давление упадет в два раза, то объем должен увеличиться также в два раза. Иными словами, половина шампанского должна вылиться. [19]
В этом разделе описываются исследования, в которых искусственный фотосинтез трактуется как установленный факт. В этих исследованиях обычно применялось освещение растворов двуокиси углерода в присутствии различных сенсибилизаторов и затем велись поиски следов формальдегида или других органических соединений с той же горячностью, с какой в свое время алхимики стремились обнаружить золото на дне тиглей. [20]
С увеличением температуры степень извлечения МЭА повышается, причем разложения МЭА почти не наблюдается. Результаты лабораторных исследований164 показали, что при отсутствии в растворе двуокиси углерода моноэтаноламин достаточно термически устойчив. [21]
Для удаления увлеченного осадком маточного раствора соль промывают легким растворителем или растворяют в воде. Из водно-щелочного раствора гидроперекись выделяют в виде мутного маслянистого слоя путем пропускания через раствор двуокиси углерода. Таким путем получается 97 - 98 % - ная техническая гидроперекись. [22]
Из 11 формально записанных уравнений только четыре можно рассматривать как независимые, характеризующиеся собственными константами равновесия. К ним относятся реакции ( 2) и ( 4) - кислотность растворов двуокиси углерода в воде, а также ( 1) и ( 7) - диссоциация воды и основность воды, причем реакция ( 7) протекает количественно и практически необратима ( протон как отдельная частица может существовать сколь-нибудь длительное время только в газовой фазе. [23]
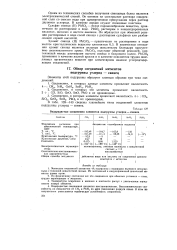 |
Водородистые соединения элементов подгруппы углерод - свинец. [24] |
Одним из технических способов получения свинцовых белил является электрохимический способ. Он основан на электролизе раствора поваренной соли со смесью соды при одновременном пропускании через раствор двуокиси углерода. В качестве анодов служат свинцовые пластины. [25]
Для сведения к минимуму этих реакций применяют большой избыток двуокиси углерода. Живой полимер либо выливают при перемешивании на твердую двуокись углерода, либо добавляют к раствору двуокиси углерода в различных растворителях, либо добавляют к газообразной двуокиси углерода, находящейся в избытке. [26]
Наблюдайте за выделением пузырьков двуокиси углерода. Когда выделение пузырьков газа прекратится, нагрейте стакан до 60 - 70 С для удаления оставшейся в растворе двуокиси углерода. [27]
Процесс восстановления двухвалентной меди в одновалентную многократно повторяется, что приводит к растворению металлической меди. Повышение температуры раствора при добавлении кислоты ускоряет растворение. Подача в раствор двуокиси углерода также способствует более быстрому растворению меди. [28]
Кристаллизация и образование твердого раствора возможны и в смесях. При сжатии таких двойных смесей при О С и давлениях выше 3300 am образуются две фазы. Одна из них - раствор двуокиси углерода в газе, а другая - твердый раствор газа в двуокиси углерода. С увеличением температуры область равновесия кристалл - газ сужается, стягиваясь к ординате чистой двуокиси углерода. С увеличением давления растворимость газа в твердой двуокиси углерода растет, а твердой двуокиси углерода в газе падает. При очень высоких давлениях, при которых может начаться кристаллизация азота или других более летучих компонентов, аналогичная картина получится и в левой части рисунка. Критическая кривая в таких системах не будет непрерывна. [29]
Реакция между двуокисью углерода и гидроксил-ионами происходит довольно медленно. Это является причиной давно известного явления: медленного исчезновения красной окраски фенолфталеина при титровании растворов двуокиси углерода. [30]
Страницы: 1 2 3