Титрованный раствор - соляная кислота
Cтраница 2
Для приготовления титрованных растворов соляной кислоты отмеряют из бюретки следующие количества концентрированной НС1 ( уд. [16]
 |
Мерная колба. [17] |
В бюретку налить титрованный раствор соляной кислоты; кончик бюретки должен быть заполнен, нижний мениск должен касаться нулевой черты. [18]
Поправки к приготовленным титрованным растворам соляной кислоты находят аналогичным образом. [19]
Почву настаивают с титрованным раствором соляной кислоты, водород которой вытесняет обменные основания. Определив остаток кислоты, вычисляют количество обменных оснований. Метод очень быстрый, но дает лишь приблизительные результаты, так как, во-первых, при однократном настаивании. [20]
Почву обрабатывают определенным количеством титрованного раствора соляной кислоты. [21]
КОН израсходовано 40 мл титрованного раствора соляной кислоты. Чему, равен титр кислоты: а) в мг-экв / мл; б) в миллиграммах НС1 на 1 мл. Сколько миллиграмм-эквивалентов ионов Н содержит 1 мл раствора кислоты. [22]
Затем растворяют осадок в титрованном растворе соляной кислоты, взятом в избытке, и отти-тровывают обратно последний по метилоранжевому, метилкрас-ному или бромтимолсинему. Определению мешает, конечно, присутствие таких элементов, как алюминий, железо или редкие земли. [23]
Временную жесткость определяют с помощью титрованного раствора соляной кислоты. [24]
Для установки титра к 10 мл титрованного раствора соляной кислоты добавляют 8 - 10 капель концентрированной азотной кислоты, 3 - 4 капли 30 % раствора нитропруссида натрия и оттитровывают раствором азотнокислой ртути до появления мути, не исчезающей в течение минуты. [25]
Содержание двуокиси углерода оценивают по количеству титрованного раствора соляной кислоты, израсходованному на реакцию с карбонатами, с последующим титрованием избытка кислорода едким натром, затем в этой же пробе титруют кальций и магний комплектном III с индикатором кислоты хром темно-синим. [26]
Гидрат окиси кальция и магния титруют титрованным раствором соляной кислоты. [27]
В методе нейтрализации чаще всего приготовляют рабочий титрованный раствор соляной кислоты, так как она является более сильной кислотой, чем серная, и переход окраски индикатора более отчетлив. Раствор соляной кислоты точной концентрации нельзя приготовить непосредственным разбавлением концентрированной НС1 ( d 1 19), которая содержит 37 % хлористого водорода, так как по плотности нельзя достаточно точно определить концентрацию раствора. [28]
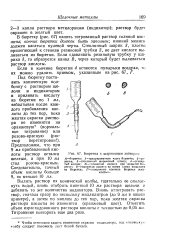 |
Бюретка с шариковым затвором. [29] |
В бюретку ( рис. 67) налить титрованный раствор соляной кислоты; кончик бюретки должен быть заполнен, нижний мениск должен касаться нулевой черты. Стеклянный шарик 3, плотно прилегающий к стенкам резиновой трубки 2, не дает кислоте выливаться из бюретки. Если сдавливать резиновую трубку у шарика 3, то образуется канал В, через который будет выливаться раствор кислоты. [30]
Страницы: 1 2 3 4