Жидкий замороженный раствор
Cтраница 1
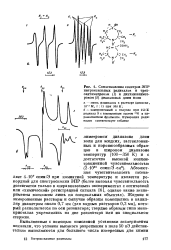 |
Сопоставление спектров ЭПР нитроксильных радикалов в трехсантиметровом ( 1 и двухмиллимет-ровом ( 2 диапазонах длин волн. [1] |
Жидкие и замороженные растворы и сыпучие образцы помещались в капилляр диаметром около 0 7 мм ( для водных растворов 0 2 мм), который располагается по оси резонатора; твердые образцы типа монокристалла укреплялись на дне резонатора или на специальном стержне. [2]
В жидких и замороженных растворах при избытке гидроксиламина скорость реакции описывается кинетическим уравнением первого порядка по ацетамиду. [3]
Было установлено, что спектры ЭПР парамагнитных ионов в жидких и замороженных растворах зависят от природы лиганда, с которым связан парамагнитный ион. Главное преимущество метода ЭПР перед физико-химическими методами исследования реакций комплексообразования заключается в том, что спектры ЭПР комплексов данного парамагнитного иона с различным числом лигандов различаются. Поэтому можно прямо наблюдать в растворе разные комплексы парамагнитного иона и тем самым исследовать реакции ступенчатого комплексообразования, определять распределение комплексов в зависимости от концентрации лиганда, рассчитывать константы устойчивости. [4]
 |
Константы скоростей реакции триэтиламина с метилиодидом в жидких и замороженных растворах ( е - диэлектрическая проницаемость растворителей, Д - криоскопическая постоянная растворителей. [5] |
Для сравнения в табл. 8.7 приведены константы скорости реакции Меншуткина в жидких и замороженных растворах. [6]
На рис. 9.4 приведены графики зависимости скорости реакции от концентрации субстрата в жидких и замороженных растворах. Как видно, зависимости скорости от концентрации 2 3-диметил - 1 4-нафтогидрохинонил - 1-фосфата в жидкой фазе при 23 5 С ( кривая /) и в замороженных растворах при - 17 С ( кривая 2) сильно различаются. [8]
Фазовое состояние каждого образца исследовали методом ЭПР в температурном интервале от точки замерзания раствора до 77 К-Спектры радикала в различных растворителях в жидких и замороженных растворах представлены в качестве примера на рис. 8.2. Во всех растворителях кроме нафталинами глицерина спектры ЭПР жидких и замороженных растворов при - 18 С представляют собой триплет. Значения тк свидетельствуют о том, что и в замороженных растворах при - 18 С радикал обладает подвижностью, сравнимой с подвижностью в жидкой фазе. [9]
Фазовое состояние каждого образца исследовали методом ЭПР в температурном интервале от точки замерзания раствора до 77 К-Спектры радикала в различных растворителях в жидких и замороженных растворах представлены в качестве примера на рис. 8.2. Во всех растворителях кроме нафталинами глицерина спектры ЭПР жидких и замороженных растворов при - 18 С представляют собой триплет. Значения тк свидетельствуют о том, что и в замороженных растворах при - 18 С радикал обладает подвижностью, сравнимой с подвижностью в жидкой фазе. [10]
 |
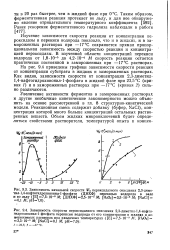
Зависимость начальной скорости окисления гидразобензола азото-кисным радикалом в диоксане от температуры ( [ R ] o [ Ci2Hi2N2 ] ol. l - 10 - 4 M. [ С2Н5ОН ] 10 - 2М. [11] |
График зависимости начальной скорости окисления гидразобензола азотокисным радикалом от температуры в жидких и замороженных растворах изображен на рис. 8.8. Как видно, эта зависимость носит экстремальный характер, причем максимум скорости реакции находится в интервале температур от - 20 до - 30 С. [12]
Вторая работа посвящена изучению механизма спинового обмена - процесса, по ряду характеристик аналогичного реакциям переноса электрона и поэтому часто используемого В. В. Воеводским для моделирования этих реакций. В работе сделан важный вывод о возможности протекания спинового обмена в концентрированных растворах по механизму, отличному от механизма соударений, о чем свидетельствует близкое совпадение для исследованных систем скоростей процесса в жидких и замороженных растворах. Результаты рассмотренных работ свидетельствуют об исключительной перспективности радиоспектроскопических методов для изучения природы слабых межмолскулярных взаимодействий и их роли в химических реакциях. [13]
Необходимо, чтобы при охлаждении активность ферментов менялась обратимо и при хранении аде происходило денатурации ферментов. Например, применение в качестве криопротекторов Сахаров предотвращает денатурацию некоторых ферментов. Для решения этих и других задач важно исследовать активность ферментов в жидких и замороженных растворах при пониженных температурах. [14]
Страницы: 1