Стандартный раствор - нитрат - торий
Cтраница 1
Стандартный раствор нитрата тория, в 1 мл раствора содержится 20 мкг тория. [1]
Стандартный раствор нитрата тория, в 1 мл раствора содержится 25 мкг тория. [2]
Стандартный раствор нитрата тория, в 1 мл содержится 20 мкг тория. [3]
Стандартный раствор нитрата тория, в 1 мл содержится 1 мкг тория. [4]
Горячий раствор титруют сначала стандартным раствором нитрата тория до красной окраски, а затем оттитровывают обратно трилоном Б до желтой. [5]
Для построения калибровочного графика в ряд мерных колб емкостью 25 мл вводят 1 - 5 мл стандартного раствора нитрата тория с содержанием Тп 5 мкг / мл, затем по 1 мл 0 05 % - ного водного раствора арсеназо III и по 8 мл концентрированной соляной кислоты ( пл. Растворы разбавляют до метки водой, хорошо перемешивают и измеряют оптическую плотность на фотоэлек-троколориметре или универсальном фотометре относительно холостого раствора. [6]
В 5 мерных колб емкостью 25 мл вносят 1 - 5 мл, с интервалом в 1 мл, стандартного раствора нитрата тория, по 2 5 мл раствора пиросульфата калия, по 2 0 мл раствора NaH2PO4 и по 5 мл раствора арсеназо II. Разбавляют растворы водой до метки, перемешивают, через 5 мин измеряют оптическую плотность и строят калибровочный график. [7]
В ряд мерных колб емкостью 25 мл вводят 1 - 5 мл, с интервалом в 1 мл, стандартного раствора нитрата тория, по 1 мл раствора арсеназо III и по 8 мл соляной кислоты. Растворы разбавляют водой до метки, хорошо перемешивают и измеряют оптическую плотность на фотоэлектроколориметре или универсальном фотометре. Для приготовления нулевого раствора берут те же растворы, но раствор соли тория не вводят. [8]
Метод заключается в обратном титровании избытка ЭДТА, не связанного в комплекс с Pu ( III) состава 1: 1, стандартным раствором нитрата тория при рН 2 5 с применением смешанного индикатора, состоящего из ализарина S и метиленового голубого. Ошибки, меньшие 1 %, получены при определении около 10 мг плутония. Определению мешают элементы, образующие прочные комплексы с ЭДТА при рН 2 5, а именно железо, титан, торий и, вероятно, галлий и ванадий. [9]
В ряд мерных колб емкостью 50 мл вводят по 2 мл раствора 1 - ( 2-пиридилазо) - резорцина, разбавляют водой до объема 10 мл и прибавляют 1 - 5 мл, с интервалом в 1 мл, стандартного раствора нитрата тория; перемешивают растворы и вводят в них по 15 мл раствора ацетата аммония. Разбавляют растворы водой до метки, хорошо перемешивают и измеряют их оптическую плотность по отношению к раствору реагента, приготовленному в аналогичных условиях. [10]
Для построения калибровочной кривой ( рис. 20) в серию мерных колб на 250 мл вводят пипеткой по 15 мл приблизительно 0 04 М раствора этилен-диаминтетрауксусной кислоты ( рН около 5) В каждую из колб добавляют 5 мл раствора хромазурола S и 60 мл воды, после чего в каждую из них вводят из бюретки различные количества стандартного раствора нитрата тория Растворы разбавляют до метки, тщательно перемешивают и измеряют их светопоглощение в ячейках ( 2 см) при 585 ммк по сравнению с дистиллированной водой. Ширина щели составляет 0 05 - 0 08 мм. Вблизи конечной точки рН каждого раствора снижается по 2 00 0 05, так как конечный объем и количество этилендиаминтетрауксусной кислоты постоянны. [11]
Большой солевой фон мешает определению тория; поэтому предварительно необходимо отделить торий от избытка минеральных кислот и их солей. Метод испытан на стандартных растворах нитрата тория различных концентраций. [12]
Объединенные водные экстракты, содержащие тории, нейтрализуют концентрированным раствором NaOH до рН 1 7 0.1. используя для контроля рН - метр Раствор переносят в мерную колб на 250 и. Избыток этиленднамннтетрауксуснон кислоты затем оттитровывают стандартным раствором нитрата тория, слегка пере-титровывая, что заметно по появлению отчетливой пурпурной окраски. [13]
Оттендорфер [171] определял цирконий и гафний в смеси их окислов следующим образом. Навеску смеси окислов переводят в раствор сплавлением с Na2S2O7 и последующим растворением плава в 1-мол. После установления рН раствора 2 5 - 3 5 ( с помощью ацетата аммония) титруют стандартным раствором нитрата тория по КО. [14]
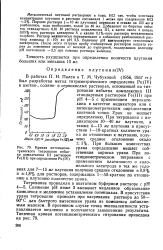 |
Кривая потенциоме-трического титрования избытка комплексона III раствором Fe ( III при определении Pu ( IV. [15] |
Страницы: 1 2