Исследованный раствор
Cтраница 4
Выведено эмпирическое уравнение для вычисления удельных объемов исследованных растворов. [46]
Тщательные опыты, при проведении которых у исследованных растворов красителей появление любых посторонних поглощающих центров было полностью устранено, действительно показали, что квантовый выход люминесценции этих веществ не зависит от длины волны возбуждающего цвета и остается постоянным не только в стоксовской, но и в антистоксовской областях спектра. [47]
Рассчитанное по уравнению (5.11) содержание септацидина в исследованных растворах приведено в четвертой части таблицы. [48]
Это указывает на то, что в исследованном растворе образуется незначительное количество внутрисферных комплексов. Основная часть сульфатного комплекса алюминия имеет внешне-сферную структуру. [49]
Приведенные данные убедительно показывают, что в исследованных растворах только железо может тормозить процесс проникновения олова в стекломассу. При окислении растворенного в олове железа снижается окислительный потенциал на межфазной границе металл - стекломасса до уровня, при котором окисление олова в интервале температур 800 - 1000 С становится термодинамически маловероятным, и, тем самым, затрудняется проникновение олова в стекломассу. [50]
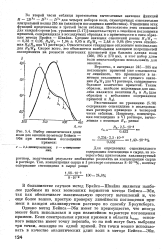 |
Выбор аналитических длин. [51] |
Рассчитанное по уравнению (5.16) содержание септацидина в исследованных растворах приведено в четвертой части таблицы. [52]
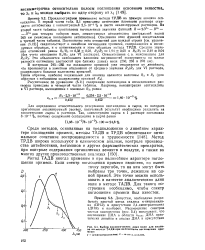 |
Выбор аналитических длин воли для анализа по методу ТАДВ при нелинейном поглощении примеси. [53] |
Рассчитанное по уравнению (5.11) содержание септацидина в исследованных растворах приведено в четвертой части таблицы. [54]
Однако нет основания считать, что в исследованном растворе преобладают анионы Cu ( CN) 2, так как в последнем случае концентрация свободного KGN должна быть соответственно большей, чем определенная экспериментально. Кроме того, данные, приведенные в табл. 1, показывают, что если даже произвести расчет концентрации ионов меди на основании наиболее обоснованной величины константы нестойкости иона Cu ( CN) 2, К 10 - 24 [141], то и в этом случае также наблюдается существенное отклонение от измеряемой величины. [55]
Из приведенных данных видно, что в исследованных растворах можно четко разграничить области плотностей тока, при которых происходит только электроосаждение палладия или совместный процесс выделения металла и водорода. Доказательством того, что в исследованных растворах ниже предельной плотности тока водород не выделяется, могут служить данные о выходах по току металла ( см. рис. 71, стр. [56]
 |
Коэфициенты диффузии в воде. [57] |
Наблюденные коэфициенты диффузии относятся к наиболее разбавленным из исследованных растворов. Вычисления были также сделаны для скоростей диффузии в воде газов: ацетилена, углекислоты, азота и водорода. В каждом случае вычисленные значения приблизительно в четыре раза больше найденных экспериментально. [58]
Полученные результаты позволяют подойти к вопросу о структуре исследованных растворов. Условие ti fl 1 означает, что за время наблюдения энергия обменного взаимодействия практически не изменяется. Таким образом, с точки зрения наблюдателя, использующего метод ЭПР, комплексы, между которыми возникает обмен, образуют в растворе долгоживущие ассоциаты ( Ti310 - 8 сек. Эти ассоциаты состоят из достаточно большого числа парамагнитных частиц ( Л 2), так как для ассоциатов с малым числом частиц рост сое в области обменного сужения линий ЭПР сопровождался бы увеличением, а не уменьшением мультиплетности спектров ЭПР. [59]
Обработка экспериментальных данных показала, что для всех исследованных растворов при низких концентрациях хорошо выполняется закон Бера. При высоких концентрациях, превышающих 1 N, наблюдаются небольшие отклонения от него, особенно заметные в спектрах растворов хлорной меди. [60]
Страницы: 1 2 3 4 5