Трехвалентный алюминий
Cтраница 2
Из таблицы видно, что одновалентные металлы - литий и натрий - имеют в среднем около одного свободного электрона на атом; трехвалентный алюминий - около трех свободных электронов; медь, которая бывает как одно -, так и двухвалентной, - несколько меньше полутора электронов на атом. [16]
Интересна также попытка Шваба [97] объяснить каталитическую активность алюмосиликатов е позиций катализа на полупроводниках, которая исходит из того, что замещение четырехвалентного иона кремния в кристаллической решетке силиката на трехвалентный алюминий равносильно введению в полупроводник акцепторной добавки, сообщающей поверхности катализатора окислительные свойства. [17]
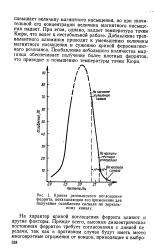 |
Кривая резонансного поглощения феррита, показывающая его применение для получения ослабления сигнала по зеркальному каналу. [18] |
При этом, однако, падает температура точки Кюри, что ведет к нестабильной работе. Добавление трехвалентного алюминия приводит к уменьшению величины магнитного насыщения и сужению кривой ферромагнитного резонанса. Прибавление небольшого количества марганца обеспечивает получение более плотных ферритов, что приводит к повышению температуры точки Кюри. [19]
Согласно закону Фарадея, образование или нейтрализация грамм-эквивалента иона требует 96 500 Кл электричества. Грамм-эквивалент трехвалентного алюминия, например, равен 9 0 г, двухвалентного свинца - 103 6 г. Это значит, что при ионизации 9 г РА освобождается такое же количество электричества, как и при ионизации 103 6 г РЬ. [20]
Кристаллическая структура глинистых минералов имеет множество дефектов. Во внутренней сетке трехвалентный алюминий нередко оказывается замещенным двухвалентным железом, магнием, кальцием, что приводит к появлению избыточного отрицательного заряда на поверхности глинистой частицы. В условиях морского осадкообразования при формировании глинистых пород заряд частицы компенсировался легкоподвижными катионами калия, натрия, кальция, магния, поэтому в естественном залегании глины нейтральны. [21]
В структуре мусковита один из каждых четырех атомов кремния в тетраэдрах замещен на алюминий. Постоянное замещение четырехвалентного кремния на трехвалентный алюминий приводит к тому, что тетраэд-рический слой в мусковите несет сильный чистый отрицательный заряд. [22]
Напротив, для химии строение кристалла является частным, притом отнюдь не важнейшим свойством вещества, а потому и не может быть принято за основу химической систематики. С точки зрения последней, трехвалентный алюминий не однотипен одновалентному серебру и двухвалентный магний - шестивалентному молибдену, а иная кристаллическая решетка Mg ( AlO2) 2 по сравнению с Са ( АЮг) 2 или NaAlO2 не может служить основанием для отнесения этих веществ к различным химическим классам. [23]
По данным Всемирной организации здравоохранения ( Jaag, 1969), после биологической очистки сточных вод из них извлекается лишь 20 - 40 % фосфора, а больше половины поступает на сброс. Фосфор рекомендуется осуждать катионами трехвалентного железа, трехвалентного алюминия или двухвалентного кальция. Каждое из этих соединений осаждает фосфор в виде нерастворимых в воде солей. Азот удаляется из сточных вод при их биологической очистке. [24]
Рассмотрим принципы метода да примере одной из изученных систем. В спектрах ядерного магнитного резонанса 170 водных растворов ( Н2170) трехвалентного алюминия имеется одиночный сигнал 170 как от координированной воды, так и от воды, оставшейся вне координационной среды. [25]
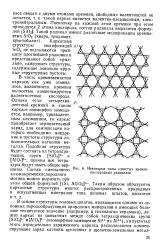 |
Некоторые типы слоистых кремие-кислородиых радикалов. [26] |
В чисто кремнеземистом каркасе, как уже отмечалось, валентности кремния полностью компенсируются валентностями кислорода. Однако если четырехвалентный кремний в таком каркасе изоморфно замещается, например, трехвалентным алюминием, то каркас приобретает отрицательный заряд, для компенсации которого необходимо внедрение в пустоты структуры дополнительных катионов металла. [27]
Хотя силикагель один не катализирует эти реакции, алюмо-спликатные катализаторы весьма активны для процессов, протекающих по механизму карбониевого иона. Считают, что это обусловлено кислотной природой поверхности смешанного окисла, в котором трехвалентный алюминий замещает четырехвалентный кремний в решетке двуокиси кремния. Природа кислотных центров и спектроскопическое доказательство их существования обсуждаются в гл. [28]
Для того чтобы выяснить причины этих осложнений, нужно проанализировать условия образования того соединения, в виде которого алюминий может раствориться в ZnS с возникновением соответствующих центров свечения. Сопоставление свойств ZnS-Cl - и ZnS-Al - фосфоров дает основание полагать, что активатором служит трехвалентный алюминий ( см. гл. III, § 2), внедряющийся скорее всего в - виде A12S3, поскольку прокаливание на воздухе с А12Оз не дает люминесцирующих препаратов. Образования А125з можно ожидать при взаимодействии H2S с А12О3, в который превращаются легко разлагающиеся кислородсодержащие соли алюминия. [29]
Полагая, что распространение кристаллографических представлений на поверхность может привести к неверным результатам, один из авторов ранее предложил модель, основанием для которой послужили электрические свойства ( поляризация) химических связей в группе А13: О: Si4 и поляризация воды с образованием водородного иона на месте активного центра. Предполагается, что на поверхности по этому механизму может соединяться самое большее три атома кремния с трехвалентным алюминием. Степень поляризации этих связей не зависит от координационного числа алюминия относительно кислорода. [30]
Страницы: 1 2 3