Коллоидный раствор - золото
Cтраница 2
При рассмотрении в ультрамикроскоп коллоидного раствора золота можно видеть необыкновенно красивую картину: беспрерывно движущиеся, переливающиеся всеми цветами радуги, разного размера частицы, из которых наиболее мелкие представляются в виде светящихся точек. [16]
При разработке методов получения коллоидных растворов золота необходимо было предусмотреть, чтобы в процессе приготовления в раствор не попадали противопоказанные примеси. [17]
Примером типичных золей могут служить коллоидные растворы золота в воде, получение которых описано ниже. В этих золях золото раздроблено до мельчайших частиц, состоящих из нескольких тысяч или даже сотен атомов золота и имеющих кристаллическую структуру. [18]
Незадолго до демонстрации опыта приготавливают коллоидный раствор золота. Полученную смесь нагревают до кипения, затем, убрав горелку, при энергичном встряхивании добавляют в нее несколько миллилитров 0 3 % - ного раствора формальдегида. В результате получается вмшнево-жрасный золь золота, который и используется в опыте. [19]
Таким образом, вопрос защиты радиоактивных коллоидных растворов золота был решен. Необходимо было далее добиться равномерной дисперсности получаемых радиоактивных золей золота. [20]
 |
Схема коллоидной мельницы. [21] |
Метод электрического распыления применяют для получения коллоидных растворов золота, серебра, платины и других металлов. [22]
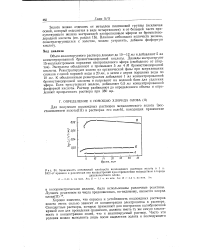 |
Зависимость оптической плотности коллоидного раствора золота в 1 н. НС1 от времени и различных его концентраций при определении посредством хлорида. [23] |
Хорошо известно, что окраска и устойчивость коллоидных растворов золота очень сильно зависит от концентрации электролитов в растворе. Стандартные растворы, которые применяют для построения калибровочной кривой или для проведения сравнения, должны иметь ту же самую кислотность и концентрацию солей, что и анализируемый раствор. [24]
В зависимости от размера и формы образующихся частиц коллоидные растворы золота имеют красный, голубой или фиолетовый цвета. [25]
В истории науки известен случай особенно высокой устойчивости коллоидных растворов золота, приготовленных Фараде-ем сто лет назад, тогда как другие золи, приготовленные в иных условиях, могут в течение нескольких минут, часов или дней разрушиться, выделяя осадок дисперсной фазы. Поэтому принято говорить лишь об относительной устойчивости коллоидов. [26]
В истории науки известен случай особо высокой устойчивости коллоидных растворов золота, приготовленных Фараде-ем сто лет назад, тогда как другие золи, приготовленные в других условиях, могут в течение нескольких минут, часов или дней разрушиться, выделяя осадок дисперсной фазы. Поэтому принято говорить лишь об относительной устойчивости коллоидов. [27]
Галецкий [4], впервые изучавший действие рентгеновских лучей на коллоидные растворы золота, установил, что при облучении изменяется их стабильность. Позднее, Батагар, Гупта, Матур [5] установили, что при действии рентгеновских лучей на золи золота, серебра, меди, гидроокиси железа и гидроокиси меди, золи, защищенные органическими веществами, не теряют стабильности, тогда как те же золи, в отсутствии органических веществ, но при достаточно высоком содержании электролитов претерпевают существенные изменения при продолжительном облучении. [28]
 |
Явление рассеяния света. [29] |
Тинда-лем ( 1869) при пропускании пучка света через коллоидный раствор золота. [30]
Страницы: 1 2 3 4