Буферный раствор - аммиак
Cтраница 1
Буферный раствор аммиака и хлорида аммония: 350 мл 25 % - ного раствора аммиака смешивают с 54 г хлорида аммония и доводят до одного литра дважды дестиллированной водой. [1]
Какая максимальная концентрация Mg возможна в 0 1 М буферном растворе аммиака при рН 10 при условии, что Mg ( OH) z не выпадает в осадок. [2]
Следует отметить, что если 2 1 ( например, в буферном растворе аммиака с хлористым аммонием), то вторичный солевой эффект в первом приближении равен нулю. [3]
Следует отметить, что если z - - l ( например, в буферном растворе аммиака с хлористым аммонием), то вторичный солевой эффект в первом приближении равняется нулю; поэтому концентрация ионов водорода в буферном растворе этого типа мало зависит от изменений концентрации соли. Аналогичный расчет применим для вычисления концентрации гидроксильного иона в растворах, содержащих слабые электролиты, причем следует помнить, что произведение концентраций ионов [ НТ ] [ ОН - ] возрастает с возрастанием ионной силы раствора. [4]
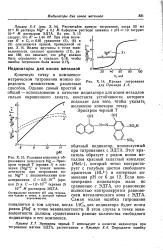 |
Кривая титрования для Примера X. 6. [5] |
Рассчитайте кривую титрования, когда 50 мл 10 - 2 М раствора Mg2 в 0 1 М буферном растворе аммиака с рН 10 титруют Ю-2 М раствором ЭДТА. [6]
Десорбцию антибиотиков осуществляют после избирательного вытеснения примесей действием водных растворов кислот, промывки колонны с сорбированным тетрациклином раствором аммония хлорида с рН 6 - 6 5, элюированием буферным раствором аммиака или борной кислоты. [7]
Израсходованный объем этого раствора отвечает содержанию кальция. Потом прибавляют 5 мл буферного раствора аммиака, около 0 1 г смеси эриохром черного Т с солью и титруют до перехода фиолетового окрашивания в синее. [8]
Значение рН раствора можно грубо регулировать добавлением кислоты или щелочи, а более точно - с помощью подходящего буферного раствора. Для этой цели часто пользуются буферными растворами аммиака и тартрата или гидроокиси щелочного металла и тартрата, который одновременно действует как маскирующий агент. Для повышения селективности осаждения можно добавлять дополнительные маскирующие агенты, такие, как ЭДТА. [9]
Образец ( около 1 мг-экв) помещают в реакционную колбу и растворяют в метаноле. Туда же вносят плоские диски из металлического кадмия и соляную кислоту и встряхивают колбу в течение 90 мин. Затем слой жидкости над дисками переносят в колбу для титрования, добавляют буферный раствор аммиака и хлорида аммония и титруют ионы кадмия 0 05 М раствором ЭДТА с эриохром черным Т в качестве индикатора. [10]
В колбу для титрования помещают 100 мл пробы. Израсходованный объем этого раствора отвечает содержанию кальция. Потом прибавляют 5 мл буферного раствора аммиака, около 0 1 г смеси эриохром черного Т с солью и титруют до перехода фиолетового окрашивания в синее. [11]
Иодид-ион сорбируется так сильно, что его трудно десорбировать. Для вымывания этого иона из колонки используют иногда мягкое окисление до свободного иода. С другой стороны, фторид-ион сорбируется очень слабо, слабее других анионов; фторид-ион вымывается из колонки соляной кислотой или гидроокисью натрия. Это свойство фторид-иона является большим преимуществом, так как дает возможность определять фтор фотометрическим методом по реакции маскирования комплекса циркония с ализарином или ализарин-комплексоном, которому мешают многие ионы ( см. гл. Методом анионного обмена при промывании колонки концентрированным раствором соляной кислоты [67] или буферным раствором аммиака с хлоридом аммония [68] фтор может быть отделен от железа, алюминия и фосфора. [12]
Страницы: 1