Нейтральный раствор - соль
Cтраница 1
Нейтральные растворы солей, 10 % - ный раствор сульфата натрия ( N3250) при температуре 20 С слабо действуют на углеродистую Ст. Алюминий в таких условиях корродирует меньше - 0 01 1 мм / год. [1]
Нейтральный раствор соли Ag4 - ( например, гальваниче - ской ванны) переводят в мерную колбу вместимостью 100мл и разбавляют водой до метки. [2]
Нейтральный раствор соли двухвалентной ртути можно титровать цианидом калия, применяя в качестве индикатора фенолфталеин до появления красного окрашивания последнего. Для таких титрований можно всегда подобрать подходящий индикатор, рассчитав предварительно кривую титрования. Изменения величины рН во время титрования вычисляют по константе ионизации той слабой кислоты ( или слабого основания), соль которой применяют в качестве титрующего реактива, и по произведению растворимости образующегося осадка или по константе ионизации получающегося мало диссоциированного соединения. Более общим случаем является титрование одного иона другим в присутствии индикатора, с которым тот или иной из этих ионов образует окрашенное вещество. Для получения хороших результатов в этих случаях необходимо, чтобы в точке эквивалентности или очень близко от нее концентрация исчезающего из раствора иона стала настолько незначительной, чтобы этот ион перестал давать окраску с индикатором, или же чтобы самая малая концентрация кона реактива ( прибавляемого в избытке) была достаточной для реакции с индикатором. Хорошо известным примером является применение соли трехвалентного железа в качестве индикатора при титровании роданидов солью серебра в кислом растворе. Роданид серебра так мало растворим, что он не дает достаточного количества ионов CNS - для реакции с ионами Fe444 в растворе, но в присутствии даже самого малого избытка ионов CNS - раствор окрашивается в красно-коричневый цвет. [3]
Из нейтральных растворов солей Y щавелевая кислота осаждает щавелевокислый иттрий Y2 ( C2O4) g 9Н2О в форме мелких палочек. [4]
К нейтральным растворам солей железа ( II), кобальта ( II) и никеля ( II) прибавляют по каплям раствор KCN ( тяга. Цианиды кобальта и никеля Ni ( CN) 2 - aq, светло-зеленый; Ni [ Ni ( CN) 4 ]) растворяются при дальнейшем добавлении KCN с образованием цианидных комплексов. [5]
К нейтральному раствору соли калия в двух пробирках прибавить в одном случае раствор гексанитритокобальтата ( Ш) натрия Ма3 [ Со ( МО2) б ], а к другой - - концентрированный раствор перхлората натрия. [6]
К нейтральному раствору соли марганца прибавляют объема насыщенного раствора щавелевой кислоты или оксалат калия и несколько капель бихромата калия. [7]
К нейтральному раствору соли марганца прибавляют раство оксалата калия и затем избыток нитрита калия. Раствор окр шивается в интенсивно красный цвет. [8]
К кислым и нейтральным растворам солей и к аммиаку плавленый кварц также вполне устойчив, однако щелочи и щелочные соли действуют на него разрушающе. К крупным достоинствам плавленого кварца следует отнести также его стойкость к резким колебаниям температуры, что объясняется его весьма малым коэфициентом расширения. Трудность изготовления крупных изделий из плавленого кварца препятствует его более широкому внедрению в химическую промышленность и до настоящего времени из этого материала изготовляется главным образом аппаратура лабораторного и полузаводского типа. [9]
К нейтральному раствору соли двухвалентного марганца в мерной колбе емкостью 100 мл прибавляют 5 мл 5 % - ного раствора комплексона, 10 мл ледяной уксусной кислоты и 0 1 г висмутата натрия. Взбалтывают в течение 1 мин. При толщине кюветы 34 мм оптимальными концентрациями Мп являются 0 1 - 1 0 лгг / 100 мл. В этих случаях получаемые окраски точно подчиняются закону Ламберта-Беера. Принимая во внимание небольшую устойчивость комплексоната марганца, рекомендуется проводить все измерения в течение первых 5 мин. О мешающем влиянии остальных катионов в общих чертах остается в силе то, что было сказано при описании колориметрического определения кобальта и хрома. [10]
К нейтральному раствору соли двухвалентного марганца в мерной колбе емкостью 100 мл прибавляют 5 мл 5 % - ного раствора комплексона, 10 мл ледяной уксусной кислоты и 0 1 г висмутата натрия. [11]
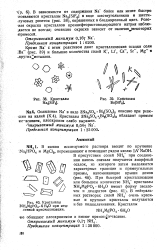 |
Кристаллы Ba [ SiFel.| Кристаллы ЗШ4МдРО4 6Н2О при медленной кристаллизации. [12] |
В нейтральных растворах солей NH4 очень красивые и крупные кристаллы получаются и без подщелачивания. [13]
В нейтральных растворах солей коррозия алюминия зависит от природы аниона. Галоидные ионы разрушают оксидную пленку. Стойкость алюминия высока в растворах солей, обладающих окислительными свойствами, таких как хромокислые и азотнокислые. Поэтому алюминий применяют в производстве аммиачной селитры и капралактама. [14]
В нейтральных растворах солей коррозия алюминия в основном определяется характером аниона. [15]
Страницы: 1 2 3 4