Концентрированный раствор - кислота
Cтраница 3
В концентрированных растворах кислот реакция протекает с переносом кислорода от углерода к фосфору и приводит к окисям первичных, вторичных и третичных фосфинов ( подробнее см. гл. Такой относительно сильный нуклеофиль-ный реагент, как диметилфосфин, не вступает в реакцию с ацетоном при нагревании до 100 - 105 С под давлением339 - зм. [31]
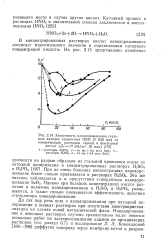 |
Зависимость наводороживания стальных катодов ( проволока ОВП 0 0 25 мм от концентрации растворов серной и фосфорной кислот ( Д 10 мА / см2, 30 мин. [32] |
В концентрированных растворах кислот наводороживание достигает максимального значения в определенном интервале концентраций кислоты. [33]
В концентрированных растворах кислот етах значительно увеличивается ( см. стр. Кроме того, найдено, что концентрацию рения можно определять в концентрированных растворах аммиака по светопоглощению перренат-иона, так как аммиак не поглощает при 230 нм. [34]
Щелочи и концентрированные растворы кислот способствуют гидролизу. [35]
При нагревании концентрированных растворов кислот и щелочей, сплавлении твердых веществ, реакциях с металлическим натрием, а также при перегонке в вакууме следует пользоваться защитными очками. [36]
При охлаждении концентрированного раствора гекса-фторкремниевой кислоты выделяется дигидрат в виде бесцветных кристаллов. В безводном состоянии кислота неизвестна. [37]
При охлаждении концентрированного раствора гек-сафторкремниевой кислоты выделяется дигидрат в виде бесцветных кристаллов. В безводном состоянии кислота неизвестна. [38]
При использовании концентрированных растворов кислот 1-я порция регенерационного раствора при фильтровании через катионит теряет большую часть кислоты, но содержание в ней вытесненных ионов кальция относительно невелико. Этот эффект возникает вследствие значительной разности между осмотическими давлениями в растворе и в набухшей смоле. Поэтому утилизация раствора, отработанного на 1 - й ступени, нецелесообразна. [39]
При охлаждении концентрированного раствора гексафторо-кремпевой кислоты ( H2SiF8) выделяется дигидрат в виде бесцветных кристаллов. В безводном состоянии кислота неизвестна. [40]
Работа с концентрированными растворами кислот сопровождается рядом неудобств: соляная кислота сильно дымит, серная-плохо выливается из измерительных цилиндров и при смешивании с водой выделяет много тепла. При разбавлении H2SO4 нарушение обычного правила-вливать кислоту в большое количество воды, а не наоборот-может привести к разбрызгиванию и сильным ожогам. [41]
При ожогах концентрированными растворами кислот обожженное место промывают сильной струей воды в течение 2 - 3 мин. При сильных ожогах следует после оказания первой помощи обратиться к врачу. [42]
При ожогах концентрированными растворами кислот обожженное место промывают сильной струей воды в течение 2 - 3 мин, затем 2 - 3 % - ным раствором соды, после чего накладывают марлевую повязку, смоченную 1 - - 2 % - ным раствором перманганата калия. При сильных ожогах следует после оказания первой помощи обратиться к врачу. [43]
При катализе концентрированными растворами кислот так же, как и в разбавленных растворах, происходит перенос протона к реагирующему веществу, однако в этом случае скорость необходимо сопоставлять не с концентрацией ионов водорода ( гидроксония), а с их активностью. [44]
Однако в концентрированном растворе кислоты коэффициенты активности необходимо учитывать. [45]
Страницы: 1 2 3 4