Концентрированный раствор - соль
Cтраница 3
В концентрированном растворе соли меди, прибавление формальдоксима и едкого кали вызывает зеленое окрашивание; приходится прибегать к разбавлению водой для того, чтобы появилось фиолетовое окрашивание. Что касается реакции, протекающей между формальдоксимом и сернокислой медью в присутствии едкого кали, то сначала я предполагал, что она тождественна с биуретовой реакцией. Однако, сравнивая их более внимательно, я отметил, что между ними имеются некоторые различия. В первую очередь, различия в окраске: окраска, вызванная формальдоксимом - черно-фиолетовая, в то время как вызванная чистым биуретом - розовая. [31]
Электролизу подвергаются концентрированные растворы солей ( около 300 г / л NaCl или 250 г. л КС1), очищенные от примесей магния и кальция. [32]
При взаимодействии концентрированных растворов солей кобальта с ионами Ag в аммиачной среде выделяется черный осадок. [33]
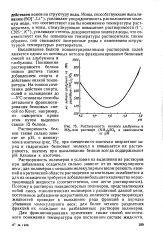 |
Растворимость яичного альбумина в. [34] |
Высаливание белков концентрированными растворами солей является одним из основных методов фракционирования белковых смесей на альбумины и глобулины. [35]
Выделение примесей из концентрированных растворов солей щелочных металлов и аммония проводили обычно на со левой форме угля ( Na, К 1, NH), соответствующей катионам анализируемого соединения. [36]
Что происходит с концентрированными растворами солей гидроксиламина в присутствии щелочей или платиновой черни. [37]
Нитрат аммония с концентрированными растворами солей четырехвалентного церия образует осадок двойной соли ( NH4) 2Ce ( NO3) 6, нерастворимой в азотной кислоте. [38]
Нитрат аммония с концентрированными растворами солей четырехвалентного церия образует осадок двойной соли ( NH4) - Ce ( NO3) B, нерастворимой в азотной кислоте. [39]
Нитрат аммония с концентрированными растворами солей четырехвалентного церия образует осадок двойной соли ( NH4) 2Ce ( NO3) 6, нерастворимой в азотной кислоте. [40]
В зернах ионита образуется концентрированный раствор соли, что влияет на гидратацию и поляризуемость ионов А В вследствие различия возникающего между свойствами концентрированного раствора внутри зерна ионита и разбавленного раствора, омывающего эти зерна. Эта теория была развита главным образом Бауманом и Эйхгорном. [41]
Ревающую роль в поведении концентрированных растворов солей, образующих кристаллогидраты, играет совокупность равновесных процессов, подготавливающих выпадение кристаллогидрата из раствора. [42]
Детали микроскопического механизма влияния концентрированных растворов солей на белки, пептиды, нуклеиновые кислоты и другие полярные растворенные вещества довольно неопределенны. Высаливание этих соединений и их составных частей, по-видимому, происходит по сложному механизму, являющемуся результатом наложения нескольких различных механизмов, как и в случае высаливания менее полярных соединений. Значения ks для полярных растворенных веществ меньше, чем для неполярных того же объема, так как полярные молекулы сильнее взаимодействуют с растворителем; при достаточно высокой полярности наблюдается всаливание. Теория, основанная на рассмотрении внутреннего давления, по-видимому, дает в настоящее время наиболее удовлетворительное объяснение высаливанию как полярных, так и неполярных веществ. [43]
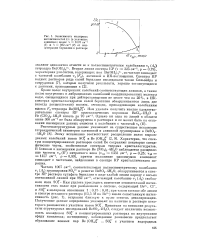 |
Зависимость молярных интенсивпостей / / с ( в условных единицах полос v 1007 см-1 ( 1 и v 982 см 1 ( 2 от концентрации бериллия в растворе. [44] |
Характерно, что спектры концентрированных растворов солей Be сохраняют некоторые специфические черты, свойственные спектрам твердых кристаллогидратов. В близком к насыщению растворе Be ( N03) 2 - 4H20 наблюдается расщепление частоты vs ( Е) нитратного иона ( v3a 1332 см 1, р 0 25; v3b 1457 см 1, р 0 89), причем положение максимумов компонент совпадает с частотами, найденными в спектре КР кристаллического порошка. [45]
Страницы: 1 2 3 4