Сравнительно концентрированный раствор - соль
Cтраница 1
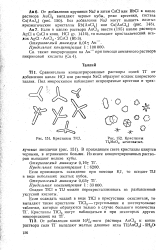 |
Кристаллы Т1С1. [ IMAGE ] Кристаллы. [1] |
Сравнительно концентрированные растворы солей ТГ от добавления капли НС1 или раствора NaCl образуют осадок хлористого таллия. [2]
 |
Кристаллы пикрата. [3] |
В сравнительно концентрированных растворах солей натрия при действии пикриновой кислоты образуется пикрат натрия, кристаллизующийся в виде розеток из тонких желтых игл ( открываемый минимум 1 yNa); осадок растворяется при добавлении капли воды. [4]
 |
Кристаллы Т1С1. [ IMAGE ] Кристаллы. [5] |
NaCl к сравнительно концентрированному раствору соли таллия ( Т1) образуется осадок хлорида таллия. [6]
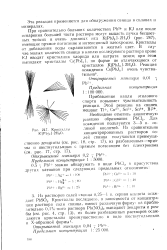
Следует отметить, что из сравнительно концентрированных растворов солей алюминия при действии одного только салицилата натрия выпадают кристаллы ( вероятно салициловой кислоты) в виде игл и узких прямоугольников ( рис. 188 6), отличающихся плеохроизмом и прямым погасанием; позже образуются более грубые иглы почти без плеохроизма и с косым погасанием. [7]
Иодат уранила бледно-желтого цвета выпадает только из сравнительно концентрированных растворов солей уранила и может быть растворен в воде. [8]
Соли серной кислоты вызывают выпадение белого осадка CaSO4 только в сравнительно концентрированных растворах солей кальция. Осадок CaSO4 растворим в ( NH4) 2SO4, а потому действием ( NH4) 2SO4 можно удалить из раствора ионы Ва ( и Sr), почти не осаждая ионов Са, что мы используем в ходе анализа. [9]
Схематическое изображение процессов, происходящих при нитевидной коррозии, представлено на рис. 15.2. Анализами показано [14], что головка нити пополняется сравнительно концентрированными растворами солей двухвалентного железа. Поэтому именно на этом участке нити имеется тенденция к абсорбции воды из атмосферы. Кислород также диффундирует через пленку, и поэтому на границе раздела между головкой и основной частью нити, а также по периметру головки достигается ( относительно поверхности металла) более высокая концентрация кислорода, чем в центре головки. [10]
 |
Кристаллы К [ РЬ ] ] - 2Н2О. [11] |
Прибавление капли этилового спирта повышает чувствительность реакции. Необходимо отметить аналогичную реакцию образования РЬСЦ. Из сравнительно концентрированных растворов солей свинца получаются преимущественно дендриты ( см. рис, 18, стр. [12]
Однако, если внести достаточное количество какого-либо другого иона, взаимодействующего с тем же реактивом и легко образующего малорастворимое соединение, то образуется осадок, состоящий из смешанных кристаллов. Примером может служить обнаружение ничтожных количеств кобальта по образованию смешанных кристаллов тетрародан-меркуриата кобальта синего цвета и бесцветных кристаллов тет-рароданмеркуриата цинка. Ионы кобальта могут образовывать осадок только из сравнительно концентрированных растворов солей кобальта. Ионы же цинка легко образуют осадок тетра-роданмеркуриата, одновременно соосаждая из раствора ничтожные количества кобальта, который окрашивает осадок в интенсивно синий цвет. [13]
Страницы: 1