Более концентрированный раствор
Cтраница 3
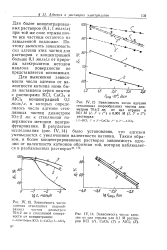
Для более концентрированных растворов из дитизоната меди и дитизона в четыреххлористом углероде Фишер [374] предложил проводить фотометрирова-ние в области длин волн 750 - 800 лцл, в которой раствор дитизона в четыреххлористом углероде и большинство других дитизонатов практически не поглощают. Однако это преимущество теряется вследствие 10-кратного уменьшения чувствительности. [31]
Плотность более концентрированных растворов измеряют по левому барабану. [32]
Для более концентрированных растворов существуют лишь полуэмпирические формулы. [33]
Для более концентрированных растворов необходимо применять метод разбавлений или производить измерения в тонких слоях. На практике часто приходится измерять люминесценцию вещества в присутствии другого поглощающего свет компонента. Второй компонент может поглощать возбуждающий свет ( экранирующий эффект) и свет люминесценции ( реаб-сорбция) и таким образом уменьшать интенсивность люминесценции и искажать ее спектр. [34]
Для более концентрированных растворов ( 0 1; I моль / л) при той же силе отрыва почти все частицы остаются на запыленной подложке. Поэтому выяснить зависимость сил адгезии этих частиц для растворов с концентрацией больше 0 1 моль / л от природы электролитов методом наклона поверхности не представляется возможным. Для выяснения зависимости числа адгезии от валентности катиона нами была поставлена серия опытов с растворами КС1, СаС12 и А1С13 концентрацией 0 1 моль / л, в которых определялось число адгезии стеклянных частиц диаметром 70 2 мк к стеклянной поверхности методом центрифугирования. В результате исследования ( рис. IV, 14) было установлено, что адгезия уменьшается с увеличением валентности катиона. [36]
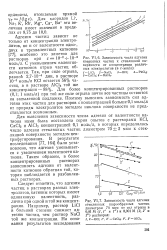 |
Зависимость числа адгезии.| Зависимость числа адгезии. [37] |
Для более концентрированных растворов ( 0 1; 1 моль / л) при той же силе отрыва почти все частицы остаются на запыленной подложке. Поэтому выяснить зависимость сил адгезии этих частиц для растворов с концентрацией больше 0 1 моль / л от природы электролитов методом наклона поверхности не представляется возможным. [38]
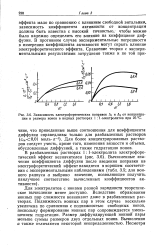 |
Зависимость электрофоретических поправок Д ] и Дз т концентрации и размера ионов в водных растворах 1. 1-электролитов при 25 С. [39] |
Для более концентрированных растворов следует учесть, кроме того, изменения вязкости и объема, обусловленные диффузией, а также гидратацию ионов. [40]
Применение более концентрированных растворов едкого жали приводит к несколько пониженным выходам. [41]
Для более концентрированных растворов ( участок 3) вновь возникает линейная зависимость от ] / С, соответствующая формуле ( 21), и кривая переходит в прямую, которая, однако, уже не проходит через начало координат и имеет другой угол наклона, зависящий от р и ех. [42]
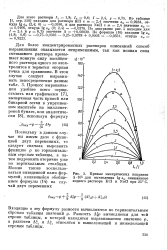 |
Кривые эмпирических поправок А 105 для вычисления lg a № смешанного водного раствора КС1 и NaCl при 25s С. [43] |
Для более концентрированных растворов описанный способ выравнивания оказывается неприменимым, так как ионная сила смешанного раствора превышает ионную силу насыщен - / Д ю5 ного раствора одного из эле к - 1601 тролитов и теряется опорная точка для сравнения. [44]
Для более концентрированных растворов кислот и щелочей пользуются только понятием нормальности. [45]
Страницы: 1 2 3 4