Сильно разбавленный раствор
Cтраница 2
Для сильно разбавленных растворов электростатическая теория пренебрегает собственными размерами ионов, рассматривая их как точечные заряды. Это вносит некоторую погрешность в выводы теории - тем меньшую, чем более разбавлен раствор. В тех случаях, когда учитывается радиус ионов, для решения поставленных задач также приходится делать известные допущения, искажающие в какой-то мере физически правдоподобную картину строения электролита. [16]
Для сильно разбавленных растворов применимо следующее правило. [17]
Для сильно разбавленных растворов электростатическая теория пренебрегает собственными размерами ионов, рассматривая их как точечные заряды. Это вносит некоторую погрешность в выводы теории - тем меньшую, чем более разбавлен раствор. В тех случаях, когда учитывается радиус ионов, для решения поставленных задач также приходится делать известные допущения, искажающие в какой-то мере физически правдоподобную картину, строения электролита. [18]
Для сильно разбавленных растворов электростатическая теория пренебрегает собственными размерами ионов, рассматривая их как точечные заряды. Это вносит некоторую погрешность в выводы теории - тем меньшую, чем более разбавлен раствор. В тех случаях, когда учитывается радиус ионов, для решения поставленных задач также приходится делать известные допущения, искажающие в какой-то мере физически правдоподобную картину строения электролита. [19]
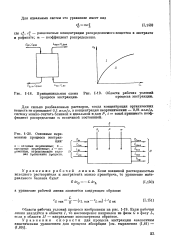 |
Принципиальная схема [ IMAGE ] - 19. Области рабочих условий процесса экстракции. процесса экстракции.| Основные переменные процесса экстракции. [20] |
Для сильно разбавленных растворов, когда концентрация органических веществ не превышает 0 1 моль / л, а концентрация неорганических - 0 01 моль / л, систему можно считать близкой к идеальной и для Р, t - const принимать коэффициент распределения m величиной постоянной. [21]
Особенности сильно разбавленных растворов должны быть связаны прежде всего со спецификой состояния внешнесферной воды в них. Совокупность приведенных данных наводит на мысль об образовании в сильно разбавленных растворах каких-то ассоциатов, обладающих относительно низкой теплоемкостью, но высокой прочностью связей и увеличенным объемом. Такими ассоциатами могут быть, например, льдоподобные кла-траты вокруг гидратированных катионов. Создается впечатление, что изученные нами электролиты, попадая в воду в очень небольшом количестве, не только не разрушают ее, но даже, наоборот, как бы слегка замораживают. Причиной этого может быть уже рассмотренная нами поляризация координационной воды. [22]
Концентрация сильно разбавленных растворов даже вполне стабильных веществ очень непостоянна и может изменяться уже при простом перемещении из одного сосуда в другой или при стоянии. Причина этих изменений заключается в сорбции компонентов смесей стенками сосудов, прокладками и пробками из резины и других материалов. [23]
Применение сильно разбавленных растворов кислоты также недопустимо, так как это ведет к заметному увеличению сопротивления в порах активных масс и затруднению формирования вследствие этого глубинных слоев паст. [24]
Для сильно разбавленных растворов электролитов следует использовать уравнение ( X. Когда неизвестны значения предельных ионных проводимостей в воде при нужных температурах, используют значения, приведенные в табл. X. С, и умножают DQ12 при 25 С на T / 334 iw, где iw - вязкость воды при температуре Т, спз. [25]
Для сильно разбавленных растворов формалина, загрязненного белковыми веществами, удобно применять метод Brochet и Cambier - воздействия на испытуемый раствор солянскислого гидроксиламина. [26]
Для сильно разбавленных растворов поглощающего вещества вдали от полос поглощения растворителя в качестве n ( v) используется значение показателя преломления растворителя. [27]
К сильно разбавленному раствору сульфата кадмия добавляют избыток ( по отношению к теоретически необходимому количеству) раствора сульфида натрия. При этом образуется лимонно-жел гый осадок сульфида кадмия. [28]
К сильно разбавленному раствору ортофосфорной кислоты ( или ее соли) добавляют аммиачный раствор хлористого аммония с хлористым магнием и слегка подогревают. Образуется белый кристаллический осадок магниево-аммиачного фосфата MgNH4PO4 - 6H2O, нерастворимого в аммиаке, но легко растворимого в разбавленных растворах минеральных кислот. [29]
В сильно разбавленных растворах практически полностью диссоциируют не только сильные, но также и слабые электролиты. В сильно разбавленных растворах очень слабых электролитов, диссоциирующих с образованием того же иона, который возникает при автодиссоциации растворителя, полной диссоциации электролита не происходит. [30]
Страницы: 1 2 3 4