Предельно разбавленный раствор
Cтраница 3
В химической практике предельно разбавленные растворы не используются, так как хотя они содержат электролит в почти полностью диссоциированном состоянии, но в таком малом количестве, что становится экономически невыгодно проводить химические реакции с участием электролитов и технически сложно наблюдать результаты этих реакций. [31]
Индекс указывает на предельно разбавленный раствор. [32]
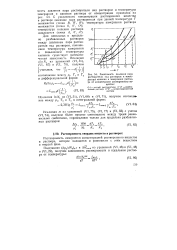 |
Зависимость давления пара растворителя над раствором и температуры кипения и замерзания раствора от концентрации растворенного вещества. [33] |
Для идеальных и предельно разбавленных растворов между давлением пара растворителя над раствором, понижением температуры замерзания и повышением температуры кипения существует математическая зависимость. [34]
Гауссовская цепочка в предельно разбавленных растворах образует клубок, имеющий форму боба. [35]
Растворенное вещество в предельно разбавленном растворе подчиняется закону Генри / 2 kx2, откуда f2 ci - & Следовательно, за стандартное состояние растворенного вещества принимается такое гипотетическое состояние чистого растворенного вещества, когда его летучесть равна константе Генри. [36]
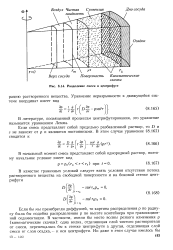 |
Разделение смеси в центрифуге. [37] |
Если смесь представляет собой предельно разбавленный раствор, то D и s не зависят от р и являются постоянными. [38]
Принятая нами для характеристики предельно разбавленных растворов картина хаотически перемешанных молекул легла в основу моделей многих теорий, например, ван - Лаара [31, 32], Гильдебранда [33] и др. Однако нам известно, что свойства далеко не всех систем могут быть описаны с помощью теорий изо-мегетичсских или регулярных растворов. [39]
Термодинамические законы и законы предельно разбавленных растворов накладывают некоторые ограничения на возможный вид функциональных зависимостей термодинамических свойств, но эти ограничения весьма общие, и с их помощью нельзя выбрать даже класс функций, в пределах которого следует искать аппроксимирующие формулы. Более конкретные рекомендации получаются с привлечением молекулярных моделей строения фазы и методов статистической термодинамики, по, естественно, область обоснованного применения таких моделей ограничена узким кругом объектов и условии. [40]
 |
Семейство кривых, описывающих первую ( тх - Т4 и вторую ( т6 закономерности осаждения Веймарна. т - время осаждения ( т, та Т3 т4 Т5. Линия г - s - граница образования типичных осадков. [41] |
В реальных условиях из предельно разбавленных растворов ( С О ОООШ) осаждение типичных Осадков вообще не происходит. Лишь с увеличением концентрации растворов до 0 001 М осадок образуется первоначально в псевдоаморфной форме, затем после очень продолжительного стояния ( до 6 месяцев) под слоем маточного раствора переходит в явно кристаллическую. Область осаждения, изучавшаяся Веймарном, находится правее пунктирной линии. При увеличении концентрации растворов от 0 001 до 1 М образующиеся осадки являются все менее совершенными с большей долей дендритных форм. [42]
Таким образом, у предельно разбавленного раствора зависимость давления пара растворителя от состава подчиняется закону Рауля, а зависимость пара растворенного вещества - закону Генри. [43]
Так, минимальный объем предельно разбавленного раствора при открытии ионов меди ( П) в виде аммиачного комплекса ( см. реакцию, приведенную выше) равен Fmin 0 05 мл при снт 4 - 10 г / мл. Это означает, что в объеме предельно разбавленного раствора, меньшем 0 05 мл, нельзя открыть ионы Си2 реакцией с аммиаком. [44]
Эта зависимость верна для предельно разбавленных растворов любых веществ. [45]
Страницы: 1 2 3 4