Электродный раствор
Cтраница 1
Электродные растворы соединены солевым мостиком из - раствора К. [1]
Колебание величины рН электродных растворов также мало сказывается на разделении данных изотопов. [2]
 |
Строение двойного электрического слоя. [3] |
Величина равновесного потенциала зависит от концентрации ионов в электродном растворе. [4]
Лабораторная установка для исследования электродиализа включает струнный электродиализатор ЭДС-Л, баки концентрата диализата и электродных растворов, три насоса с переменной производительностью, электропульт; габаритные размеры 1230 X 555 X X 640 мм. [5]
 |
Схема гальванической цепи при потенциометрическом титровании. [6] |
Электрод сравнений и Исследуемый раствор соединяют при помощи элактролитического моста, обеспечивающего электролитическую проводимость между электродными растворами, но препятствующего их взаимной диффузии. Электролитический мост представляет собой изогнутую стеклянную трубку, заполненную агар-агаром, содержащим хлорид калия. [7]
Электрод сравнения и исследуемый раствор соединяют с помощью электролитического моста, обеспечивающего электролитическую проводимость между электродными растворами, но препятствующего их взаимной диффузии. Электролитический мост представляет собой изогнутую стеклянную трубку, заполненную агар-агаром, содержащим хлорид калия. [8]
 |
Электроды, применяемые при измерении рН. [9] |
В основе потенциометрических методов лежит зависимость потенциала электродов от активности ионов определенного вида, находящихся в электродном растворе. [10]
Солевой сифон ( или электролитический мостик), наполненный насыщенным раствором хлорида калия, обеспечивает электрическую проводимость между электродными растворами, но препятствует их взаимной диффузии. Звенья этой цепи соединены инертными платиновыми электродами Pti и Ptn и металлической проволокой. Ионы Fe приобретают по одному электрону у электрода, опущенного в раствор соли железа ( III), и восстанавливаются в Ре - ионы; а Си-ионы отдают по одному электрону у электрода, опущенного в раствор соли меди ( I), и окисляются в Си4 - ионы. Платиновый электрод Ptj заряжен отрицательно, платиновый электрод Ptn - положительно. [11]
Солевой сифон ( или электролитический мостик), наполненный насыщенным раствором хлорида калия, обеспечивает электрическую проводимость между электродными растворами, но препятствует их взаимной диффузии. Звенья этой цепи соединены инертными платиновыми электродами Pti и Ptn и металлической проволокой. Ионы Ре приобретают по одному электрону у электрода, опущенного в раствор соли железа ( III) и восстанавливаются в Ре - ионы; а Си - ионы отдают по одному электрону у электрода, опущенного в раствор соли меди ( I), и окисляются в Си - ионы. Платиновый электрод Pti заряжен отрицательно, платиновый электрод Ptn-положительно. [12]
 |
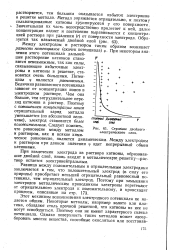
Потери аминокислот после 70 % - ного обессоливания раствора. [13] |
Сравнивая данные, полученные Блейни и Уардли, с данными Пирса, можно заключить, что первые неправильно выбрали состав электродных растворов. Если аминокислота мигрирует в катодную секцию, то кислая среда только благоприятствует ее переносу, увеличивая потери обессоливания. [14]
По отношению к ним устанавливают потенциалы индикаторных электродов, собранных для определения активности потенциалопределяющих ионов, которые входят в состав их электродного раствора. [15]
Страницы: 1 2