Красно-фиолетовый раствор
Cтраница 2
Опр ед елени13 цианидав в Г2рькр шндальяоЙ воде / 43 / 1 5 мл горькоминдальной воды разбавляют водой до 25 мл, прибавляют I мл аммиака мурексид и титруют красно-фиолетовый раствор 0 01 М раствором сульфата никеля. Перед точкой эквивалентности смесь окрашена в оранжево-красный цвет, который переходит от одной капли титранта в желтый. Метод дает точные результаты. [16]
Смесь перемешивают в течение 2 ч, нагревая ее при этом до 50 - 60 С. Красно-фиолетовый раствор оставляют на ночь, после чего его экстрагируют эфиром. Темно-красный экстракт нейтрализуют бикарбонатом натрия, при этом он приобретает желтую окраску. После высушивания над сульфатом натрия и перегонки получают г ( 54 %) жидкости, кипящей в интервале 108 - 112 С / 6 мм. [17]
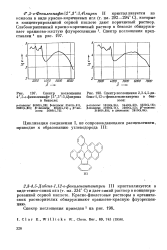 |
Спектр поглощения 2 3 - 4 5-дж-бенз - 1 12-о-фениленантантрена в бензоле. [18] |
С) и дает синий раствор в концентрированной серной кислоте. Красно-фиолетовые растворы в органических растворителях обнаруживают оранжево-красную флуоресценцию. [19]
 |
Окраска растворов продуктов реакции и значение Я Макс. [20] |
Оптическую плотность полученного красно-фиолетового раствора измеряют при зеленом светофильтре. Окраска устойчива в течение 30 мин. [21]
На платиновом аноде он окисляется в две одноэлектронные вольт-амперометрические стадии. Сначала образуется катион-радикал ( красно-фиолетовый раствор), который, по данным ЭПР-спектро-скопии, способен существовать - 1 ч после прекращения электролиза. На второй стадии образуется продукт красного цвета. Под-кисление раствора затрудняет окисление. Если в раствор ввести основание - дифенилгуанидин, то первая волна не изменяется, а вторая искажается, возможно, вследствие образования осадка на электроде. [22]
Смешивают 1 мл хлороформного раствора, содержащего 25 - 200 мкг холестерина, с 1 мл 5 % - ного раствора безводного А1С13 в нитробензоле, нагревают 1 ч при 50 С, быстро охлаждают до 20 - 30 С и вводят 1 мл 5 % - ного раствора анисового альдегида в смеси равных объемов бензола и нитробензола. Через 30 мин добавляют смесь бензола и нитробензола до объема 10 мл и оптическую плотность красно-фиолетового раствора измеряют при 536 нм. [23]
Лактаровиолин Лактаровиолин является единственным известным в настоящее время антибиотиком-азуленом. Он хорошо растворим в большинстве органических растворителей ( особенно легко в СНС13 и пиридине), давая красно-фиолетовые растворы с фиолетовой флуоресценцией. [24]
Ализарин кристаллизуется в красных иглах ( темп, плавл. В воде ализарин почти нерастворим, немного растворяется в спирте; как фенол он легко растворяется в едких щелочах, давая интенсивно окрашенные красно-фиолетовые растворы. [25]
Ализарин кристаллизуется в красных иглах ( темп, плавл. В воде ализарин почти нерастворим, к9 много растворяется в спирте; как фенол он легко растворяется в едких щелочах, давая интенсивно окрашенные красно-фиолетовые растворы. [26]
Расстояние между точками ветвления составляет 18 - 27 остатков глюкозы, причем в крахмале, в отличие от гликогена ( см. далее), таких разветвлений относительно немного. Молекулы амилопектина имеют сферическую форму с радиусом вращения 82 - 255 нм и молекулярной массой от 100 тыс. до нескольких миллионов. Взаимодействие с иодом приводит к образованию красно-фиолетовых растворов, позволяющих отличить фракцию амилопектина от фракции амилозы. При ферментативном гидролизе амилопектина а-амилазами образуется остаточный декстрин, причина образования которого состоит в том, что амилазы являются а - ( 1 4) глкжозидазами и не расщепляют 1 6-гликозидные связи. Остаточный декстрин представляет собой крупный, сильно разветвленный остов полисахарида. При его дальнейшем распаде образуется изомалътоза - 6 - ( а - О-глюколиранозидо) - О-глюкопираноза - превращение которой в глюкозу требует применения специфической а-1 6-глюкозидазы. Водные растворы декстринов окрашиваются иодом в красный цвет. [27]
Расстояние между точками ветвления составляет 18 - 27 остатков глюкозы, причем в крахмале, в отличие от гликогена ( см. далее), таких разветвлений относительно немного. Молекулы амилопектина имеют сферическую форму с радиусом вращения 82 - 255 нм и молекулярной массой от 100 тыс. до нескольких миллионов. Взаимодействие с иодом приводит к образованию красно-фиолетовых растворов, позволяющих отличить фракцию амилопектина от фракции амилозы. При ферментативном гидролизе амилопектина а-амилазами образуется остаточный декстрин, причина образования которого состоит в том, что амилазы являются а - ( 1 4) глкжозидазами и не расщепляют 1 6-гликозидные связи. Остаточный декстрин представляет собой крупный, сильно разветвленный остов полисахарида. При его дальнейшем распаде образуется изомааътоза - 6 - ( а - О-глкжолиранозидо) - В-глюкопираноза - превращение которой в глюкозу требует применения специфической а-1 6-глюкозидазы. Декстрины могут быть получены также при обработке крахмала 10 % - ным водным раствором серной кислоты ( так называемая декстринизация крахмале. Водные растворы декстринов окрашиваются иодом в красный цвет. [28]
Предварительно были изучены некоторые свойства комплекса германия с ПФ без желатины. Оптическая плотность красно-фиолетового раствора в присутствии и в отсутствие буферного раствора одинакова, поэтому нет оснований предполагать, что компоненты буферного раствора входят в состав соединения. [29]
В пробирку отбирают 6 0 мл дистиллята, добавляют 0 5 мл раствора хромотроповой кислоты, 5 мл концентрированной серной кислоты и все это перемешивают. Пробирку помещают на кипящую водяную баню. Через 30 мин содержимое пробирки охлаждают до комнатной температуры и разбавляют дистиллированной водой до 20 0 мл. После перемешивания измеряют оптическую плотность образовавшегося желто-красного или красно-фиолетового раствора, пользуясь кюветами с толщиной слоя 5 см и зелеными светофильтрами ( Я. Вычитают значение оптической плотности холостого определения с дистиллированной водой. По калибровочной кривой находят содержание формальдегида. [30]
Страницы: 1 2 3