Водный раствор - хлористый натрий
Cтраница 1
Водный раствор хлористого натрия, содержащий небольшое количество примесей, течет к электролитической ячейке через подвергающуюся коррозии трубу из сплава железа, а затем через коррозионно-стойкую трубу из органического пластика. Ток утечки, от ячейки через раствор в трубе, составляющий 0 57 А, вызвал нежелательную коррозию трубы из сплава железа. Инертный в коррозионном отношении металлический электрод, потенциал которого больше, чем у железа, помещали в пластиковой трубе и соединяли с землей. [1]
Электролиз водных растворов хлористого натрия дает возможность получать хлор, водород и едкий натр. [2]
Помимо водных растворов хлористого натрия, хлористого магния и хлористого кальция в качестве эвтектиков применяют и другие растворы. [3]
Если в водный раствор хлористого натрия погрузить сильнокислотный катионит в натриевой форме, то окажется, что концентрация хлористого натрия внутри зерен катионита будет значительно ниже, чем во внешнем растворе. Это произойдет потому, что концентрация подвижных ионов натрия в катиони-те высока и ионы натрия из внешнего раствора не могут в значительной степени проникнуть внутрь зерна. Концентрация ионов хлора в зерне в начальный период погружения равна нулю, поэтому ионы хлора будут стремиться проникнуть внутрь зерна, но вследствие закона электронейтральности это может быть достигнуто только в том случае, если с анионом внешнего раствора в зерно будут проникать катионы натрия. [4]
Рассолы - водные растворы хлористого натрия Nad и хлористого кальция СаСЬ применяют для температур охлаждаемой среды, близких к нулю или ниже его. [5]
При электролизе водных растворов хлористого натрия или хлористого калия на твердом катоде ( угольном или металлическом) всегда выделяется водород. [6]
При электролизе водных растворов хлористого натрия возможен также разряд ионов гидроксила и молекул воды. [7]
При электролизе водных растворов хлористого натрия на твердых катодах протекает выделение водорода. [8]
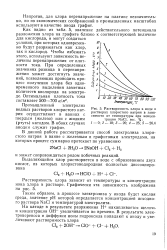 |
Растворимость хлора в воде и растворах хлористого натрия в зависимости от температуры при концентрации NaCl, вес. %. 1 0. 2 - 10. 3 - 20. 4 - 25. 5 - 26 4. [9] |
Промышленный электролиз водных растворов хлористого натрия осуществляют в ваннах с твердым ( железо) или с жидким ( ртуть) катодом. В обоих случаях анодом служит графит. [10]
Получается электролизом водного раствора хлористого натрия, также взаимодействием раствора соды с известковым молоком или прокаливанием смеси кальцинированной соды с окисью железа и дальнейшим разложением феррита натрия водой и упариванием раствора едкого натра. [11]
Получается электролизом водного раствора хлористого натрия, также взаимодействием раствора соды с известковым молоком или прокаливанием окиси железа с содой и дальнейшим разложением феррита натрия водой. [12]
При электролизе водных растворов хлористого натрия только часть его превращается в едкий натр. [13]
При электролизе водного раствора хлористого натрия в случае, когда электроды электролизера не разделены диафрагмой, в результате вторичной реакции образуется гипохлорит натрия - На аноде вследствие частичной разрядки ОН-ионов помимо хлора выделяется также небольшое количество кислорода. [14]
При электрохимическом разложении водных растворов хлористого натрия в ваннах с твердым катодом необходимо отделять анодный продукт электролиза-хлор от катодного продукта - едкого натра. [15]
Страницы: 1 2 3 4