Водный раствор - хлор
Cтраница 2
Влажный хлор, а также водный раствор хлора - хлорная вода, обесцвечивают большинство красящих органических веществ. Объясняется это тем, что хлор частично реагирует с водой, образуя наряду с соляной кислотой хлорноватистую кислоту С1гЧ - HjO HCl HC1O, которая окисляет красящие вещества и тем самым их разрушает. [16]
Составить уравнения реакций, в которых водные растворы хлора, брома и иода проявляют окислительные свойства. [17]
Хлоргидринный метод включает гипохлорирование пропилена в водном растворе хлора, омыление пропиленхлоргидрина гидратом окиси кальция и выделение окиси пропилена. Для процесса получения окиси пропилена хлоргидринным методом характерны высокий расход сырья и значительные количества неиспользованных отходов. Преимуществом же этого метода является возможность полного использования оборудования, смонтированного для производства окиси этилена. [18]
В настоящее время сточные воды обеззараживают главным образом водным раствором хлора, а при производительности очистной станции до 1000 м3 / сут - и хлорной известью. [19]
В работе [2] разрадботана и представлена математическая модель реакции между водным раствором хлора и активным углем. Модель учитывает уменьшение скорости реакции в результате поверхностных и диффузионных явлений при накоплении продуктов реакции. Параметры модели были определены при анализе данных, полученных для лабораторных реакторов периодического действия, и потом их использовали для описания зависимости концентраций хлора от времени для углей различной зернистости, различных концентраций хлора и содержания угля в реакторах. Модель была затем использована для изучения зависимости концентрации хлора в воде от времени для проточного реактора с неподвижным слоем угля. Применимость модели к обоим типам реакторов была проверена лабораторными экспериментами. [20]
В отличие от озонирования взаимодействие органических веществ с активным хлором ( водными растворами хлора, содержащими С12, НОС1, ОС1 -) является типичным гомофазным, гомогенным процессом. [21]
В промышленных процессах применяют не хлорноватистую кислоту, а гипохлориты в кислой среде или водный раствор хлора, которые, помимо хлоргидрина, неизбежно ведут к образованию хлор-производных этилена. [22]
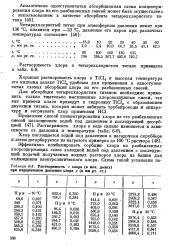 |
Растворимость с хлора ( в иол. долях при парциальной давлении хлора р ( в им рт. ст. [23] |
Эффективно комбинировать сорбцию хлора из разбавленных хлорсодержащих газов холодной водой под давлением с последующей подачей получаемых водных растворов хлора на башни для охлаждения электролитического хлора. [24]
Надо только отметить, что эти расчеты применимы для оптимальных условий: при растворении золота в водных растворах хлора они должны содержать достаточное количество НС1, а при растворении в водных растворах брома и иода - необходимый избыток соответствующей галоидной соли. [25]
Принимая во внимание значение этих вопросов для рациональной организации процессов обесцвечивания воды хлором, мы провели систематические исследования взаимодействия водных растворов хлора с некоторыми растительными экстрактами, а также водой рек, водохранилищ и прудов. [26]
Полагают [9], что окислительное действие газообразных хлора и диоксида серы на древесину ели в основном подобно реакциям с кислыми растворами сульфита и водными растворами хлора. [27]
 |
Некоторые константы равновесия. [28] |
Качественный анализ на бромиды и иодиды в присутствии хлоридов и фторидов можно выполнить очень быстро в одном растворе, основываясь на том, что медленное добавление к такому раствору водного раствора хлора приводит прежде всего к окислению бесцветных иодид ионов в обладающий заметной окраской иод. При дальнейшем добавлении водного раствора хлора окрашенный иод окисляется в бесцветные иодат-ионы, я затем происходит окисление бесцветных бромид-ионов в окрашенный бром. [29]
Первые заключения о химическом составе угля, основанные на реакциях его с галоидами, были сделаны еще в 1881 г., когда Бе-ван и Кросс [1] сообщили, что кеннельский уголь при обработке его водным раствором хлора превращается в бурый продукт, полностью растворяющийся в водном растворе едкого кали с образованием темнобурого раствора, из которого при нейтрализации минеральной кислотой выделяется хлопьевидный осадок. Осадок этот имел сходство с продуктом обработки водным раствором хлора одеревеневших волокон и обугленной серной кислотой целлюлозы, и авторы считали вероятным, что целлюлоза, лигнин, торф, бурый уголь, кеннельский уголь и антрацит являются членами обширного ряда соединений, претерпевших изменения в природных условиях. Те же авторы [2] указывали, что уголь при обработке его разбавленной соляной кислотой и хлорноватокислым калием становится полностью растворимым в щелочи. Было также найдено, что восстанавливающее действие всех углеродистых веществ ( включая, вероятно, и угли) на серную кислоту с образованием сернистой кислоты обратно пропорционально содержанию в них углерода и что действие это совершенно исчезает после прокаливания этих веществ в струе хлора. Смит [3] изучал продукты обработки угля разбавленной соляной кислотой и хлорноватокислым калием. [30]
Страницы: 1 2 3 4