Кислый водный раствор
Cтраница 3
ЧТОБ кислых водных растворах альдозы и кетозы образуют при конденсации л актольной гидроксильной группы с другими гид-роксилами внутренние гликозиды, или гликозидные ангидриды ( ср. В случае гексоз и гепту-лоз в равновесии сахар ангидрид вода, возможно, участвуют 1 6-ангидрогексопиранозы и 2 7-ан-гидрогептулопиранозы соответственно. Хотя в принципе возможны и другие ангидриды, например ангид-рофуранозы, их свободная энергия обычно высока и участие в равновесии незначительно. Другие потенциально возможные циклические системы с трех-и четырехчленными кольцами имеют настолько высокие свободные энергии, что в дальнейшем рассматриваться не будут. [31]
В кислых водных растворах ацил - и диацилферроцены, ферроцен-альдегид, фенилферроцен, а-пиридил - и а-хинолилферроцен, ферроце-пиламин ц N-алкилферроцениламины разлагаются с образованием производных циклопентадиена, не содержащих железа. [32]
В кислых водных растворах ацил - и диацилферроцены, ферроценальде-гид, фенилферроцен, а-пиридил - и а-инолилферроцен, ферроцениламшг и N-алкилферроцениламины разлагаются с образованием производных цикло-пентадиеыа, не содержащих железа. [33]
В кислых водных растворах ацил - и диацилферроцены, формилферро-цен, фенилферроцен, а-пиридил - и а-хинолилферроцен, ферроцениламин и N-алкилферроцениламины разлагаются с образованием производных цик-лопентадиена, не содержащих железа. [34]
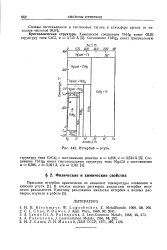 |
Иттербий - ртуть. [35] |
В кислых водных растворах амальгамы иттербия энергично разлагаются. [36]
В сильно кислых водных растворах цианамид очень быстро превращается в мочевину; то же самое превращение, но только с меньшей скоростью, протекает в сильно щелочных растворах. Это же превращение происходит, когда кальций-цианамид вводят в почву или применяют во многих органических и неорганических смесях, и этой именно реакцией объясняется применение цианамида в земледелии. [37]
В нейтральном и кислом водном растворе наблюдается гибель анион-радикалов по второму порядку. [39]
В кислых водных растворах ароматических диазосоединений свободные нейтральные радикалы обычно 1 не образуются, но в некоторых неводных средах, в меньшей степени благоприятствующих ионной диссоциации, их образование представляется вероятным. [40]
В нейтральном и кислом водном растворе наблюдается гибель анион-радикалов по второму порядку. [42]
При нагревании кислых водных растворов L-сорбозы процесс распада идет в сторону образования оксиметилфурфурола, затем муравьиной и левулиновой кислот; при рН ниже 3 0 наступает процесс реверсии, который идет параллельно с процессом дегидратации и образования оксиметилфурфурола. [43]
При электролизе кислых водных растворов кетонов иногда происходит образование металлоорганических соединений. [44]
При реакции кислого водного раствора бихромата калия с метанолом раствор изменяет цвет от светло-оранжевого до грязно-зеленого вследствие образования иона Сг3, окрашенного в зеленый цвет. Следует отметить, что между углеродом и кислородом существует двойная связь ( см. раздел 16 - 5) и что все атомы расположены в одной плоскости. [45]
Страницы: 1 2 3 4