Насыщенный раствор - различное вещество
Cтраница 1
Насыщенные растворы различных веществ резко различаются по концентрации. У хорошо растворимых ве-ществ насыщенные растворы обладают высокой концентрацией растворенного вещества, а у малорастворимых концентрация насыщенного раствора невелика. [1]
Концентрация насыщенных растворов различных веществ, выраженные в граммах на литр, близки между собой по порядку величин. Поэтому соответствующие молярные концентрации оказываются тем меньше, чем больше молекулярная масса растворенного вещества. Поскольку с помощью измерений осмотического давления можно определить молекулярную массу в весьма разбавленных растворах, этот метод особенно удобен для исследования высокомолекулярных соединений. Он обладает большими преимуществами также по той причине, что изготовление подходящей мембраны оказывается тем проще, чем больше различаются размеры молекул растворенного вещества и растворителя. [2]
Поэтому концентрация насыщенных растворов различных веществ имеет разную величину. [3]
Значения ks при 20 и 80 С для насыщенных растворов различных веществ приведены в табл. 5 Приложения. [4]
Для определения удельной адсорбции паров воды эксикатор-ным методом требуется несколько ( по числу точек изотермы) эксикаторов с насыщенными растворами различных веществ, воздушный термостат и бюксы с хорошо прошлифованными крышками. Каждая точка изотермы адсорбции определяется в отдельном эксикаторе, в котором с помощью воздушного термостата поддерживают определенную температуру и давление. Исследуемый адсорбент ( около 1 г), предварительно обезвоженный в эксикаторе с хорошим осушителем ( Ps05, СаСЬ, силикагель) или термообработкой, помещают ( в бюксе с открытой крышкой) в эксикатор и выдерживают в нем до постоянного веса. Удельную адсорбцию рассчитывают делением количества адсорбированной воды на навеску адсорбента. Следует помнить, что при взятии навески и по-следущих взвешиваниях бюкса продолжительный контакт адсорбента с воздухом недопустим. [5]
Для определения удельной адсорбции паров воды эксикатор-ным методом требуется несколько ( по числу точек изотермы) эксикаторов с насыщенными растворами различных веществ, воздушный термостат и бюксы с хорошо прошлифованными крышками. Каждая точка изотермы адсорбции определяется в отдельном эксикаторе, в котором с помощью воздушного термостата поддерживают определенную температуру и давление. [6]
Для определения удельной адсорбции паров воды эксикатор-ным методом требуется несколько ( по числу точек изотермы) эксикаторов с насыщенными растворами различных веществ, воздушный термостат и бюксы с хорошо с прошлифованными крышками. Каждая точка изотермы адсорбции определяется в отдельном эксикаторе, в котором с помощью воздушного термостата поддерживают определенную температуру и давление. Исследуемый адсорбент ( около 1 г), предварительно обезвоженный в эксикаторе с хорошим осушителем ( Р2О5, СаСЬ, силикагель) или термообработкой, помещают ( в бюксе с открытой крышкой) в эксикатор и выдерживают в нем до постоянного веса. Удельную адсорбцию рассчитывают делением количества адсорбированной воды на навеску адсорбента. Следует помнить, что при взятии навески и по-следущих взвешиваниях бюкса продолжительный контакт адсорбента с воздухом недопустим. [7]
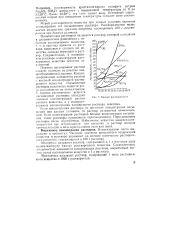 |
Кривые растворимости. [8] |
Понятие насыщенный раствор следует отличать от понятия концентрированный раствор. Концентрированным называется раствор с высокой концентрацией растворенного вещества. Насыщенные растворы различных веществ резко различаются по концентрации. [9]
Разумеется, понятия насыщенный и концентрированный не тождественны. Например, 35 % - ный водный раствор КВг является концентрированным, но он ненасыщен, так как при 20 С в 100 г воды растворяется около 65 8 г КВг. Наоборот, насыщенный раствор сульфата кальция при 20 С на каждые 100 г воды содержит всего 0 2 г CaSO4; сказывается малая растворимость этого вещества: раствор будет насыщенным, но весьма разбавленным. Так как насыщенные растворы различных веществ охватывают концентрации от ничтожно малых до весьма значительных, то они подобны лишь с формальной стороны. Их структура может быть самой разнообразной - от почти неискаженного строения чистого растворителя до структуры, близкой к кристаллической решетке растворенного вещества. [10]
Разумеется, понятия насыщенный и концентрированный не тождественны. Например, 35 % - ный водный раствор КВг является концентрированным, но он ненасыщен, так как при 20 С в 100 г воды растворяется около 65 8 г КВг. Наоборот, насыщенный раствор сульфата кальция при 20 С на каждые 100 г воды содержит всего 0 2 г CaSO4; сказывается малая растворимость этого вещества; раствор будет насыщенным, но весьма разбавленным. Так как насыщенные растворы различных веществ охватывают концентрации от ничтожно малых до весьма значительных, то они подобны лишь с формальной стороны. [11]
Итак, растворимость данного вещества отвечает величине его концентрации в насыщенном растворе. Она определяется энтальпийным и энтропийным факторами. Для разных веществ состояние истинного равновесия в растворах может наступить при различных соотношениях между ними. Это связано с различной природой растворенного вещества и растворителя, с неодинаковой интенсивностью взаимодействия их частиц и др. Поэтому концентрация насыщенных растворов различных веществ имеет разную величину. [12]
Страницы: 1