Растворение - хромовый ангидрид
Cтраница 2
Хромовый ангидрид был 97 % - ной чистоты. При растворении хромового ангидрида в уксусном ангидриде раствор необходимо охлаждать. При прибавлении уксусного ангидрида к твердому хромовому ангидриду может произойти разложение со взрывом. Следует прибавлять хромовый ангидрид к охлажденному уксусному ангидриду и при этом небольшими порциями. [16]
В результате растворения хромового ангидрида в воде образуется смесь полихромозых кислот: бихромовой при средней концентрации СгО3 и три - и тетрахромовой пр и увеличенной концентрации. Помимо большой концентрации СгО3 тетрахромовый электролит характеризуется еще и введением в него едкого натра, необходимого для образования тетрахромата натрия. Содержание едкого натра в некотором оптимальном количестве способствует получению качественных осадков с максимальным выходом по току. Рекомендуется следующий состав и режим тетрахроматного электролита ( г / л) [104]: СЮ3 350 ч - 400; H2SO4 2 0 ч - 2 5; NaOH 40 - т - 60; сахар или глюкоза 1 - 2; режим хромирования: DK 10 ч - 80 А / дм2, / 18 ч - 22 С. Сахар или глюкоза вводится в электролит для образования трехвалентного хрома, оказывающего влияние на внешний вид и качество осадка. [17]
Хромовая кислота в чистом виде неизвестна и существует только в растворе, получаемом путем растворения хромового ангидрида СгО3 в воде. [18]
Процесс электролитического хромирования имеет целый ряд отличительных черт по сравнению с другими гальваностегическими процессами. В качестве главного компонента раствор ванны хромирования содержит не соль наносимого металла, как в большинстве применяемых электролитов, а хромовую кислоту, получаемую растворением хромового ангидрида в воде. Применение такого электролита вызвано тем, что удовлетворительный осадок из растворов солей двух - и трехвалентного хрома получить трудно. В настоящее время хромирование ведется из ванн, содержащих раствор хромового ангидрида ( СгО3) с небольшой добавкой серной кислоты. [19]
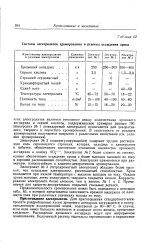 |
Составы электролитов хромирования и режимы осаждения хрома. [20] |
Для приготовления стандартного электролита раздробленные куски хромового ангидрида загружаются в ванну, наполненную водопроводной водой, подогретой до 60 - 80 С. В случае, если вода имеет большую жесткость и содержит много железа, применяют конденсат. Растворение хромового ангидрида ведут при непрерывном помешивании. [21]
Это типичный кислотный окисел; ему соответствуют две кислоты - хромовая Н2СгО4 и двухромовая Н2Сг2О7, существующие только в водном растворе. Они образуются при растворении хромового ангидрида в воде. [22]
В качестве катодов применяют пластины рольного свинца. Конструктивно ванны электрополирования одинаковы с ваннами хромирования. Составлять электролит начинают с растворения хромового ангидрида в небольшом объеме воды. Затем приливают фосфорную кислоту, после чего при перемешивании постепенно вводят серную кислоту, доводят добавками воды или выпариванием электролит до уд. [23]
 |
Неполадки при электрополировании стали и способы их устранения. [24] |
В качестве катодов применяют пластины рольного свинца. Конструктивно ванны электрополирования одинаковы с ваннами хромирования. Составление электролита производят начиная с растворения хромового ангидрида в небольшом объеме воды. Затем приливают фосфорную кислоту, после чего при перемешивании, постепенно, вводят серную кислоту, доводят добавками воды или выпариванием, плотность электролита до 1 74 г / см3 и прогревают при 383 - 393 К. [25]
Страницы: 1 2