Растворение - кальцит
Cтраница 2
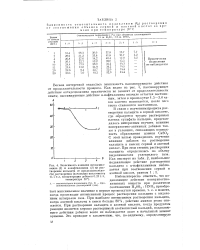 |
Зависимость влияния октадециламина ( 1 и а-нафтиламина ( 2 на растворение кальцита от продолжительности растворения ( начальная кислотность г / л, концентрация добавок г / л, температура 20. [16] |
При наиболее интенсивном растворении кальцита, когда азотной кислоты в смеси больше 80 %, действие аминов резко снижается. При растворении кальцита в азотной кислоте, когда продуктом реакции является хорошо растворимый азотнокислый кальций, подавляющего действия добавок вовсе не наблюдается даже в начальный момент времени. [17]
Кроме наклона стакана, необходимы другие предосторожности: к навеске прибавляют относительно большой объем воды, кислоту добавляют медленно; это помогает образованию слоя относительно концентрированного раствора у самого дна стакана. При растворении кальцита нужно избегать перемешивания содержимого стакана. [18]
В присутствии октадециламина ( аналогичная картина наблюдается и для а-нафтиламина) растворение кальцита в тех же пределах кислотности меняется сравнительно незначительно. Уменьшение скорости растворения кальцита с ростом концентрации серной кислоты связано с более благоприятными условиями образования пленки CaS04 в концентрированных растворах H2S04, экранирующей поверхность кальцита. При этом наибольшее подавление наблюдается при наивысшей скорости растворения кальцита. [19]
При температуре выше 60 эффект подавления снова возрастает. Поскольку в процессе растворения кальцита на его поверхности образуется трудно растворимая пленка CaS04, то нет оснований считать диффузию определяющей процесс, хотя, как известно, температурный режим влияет на изменение условий диффузии. Можна предположить, что с изменением температуры среды меняется структура кристаллов сульфата кальция на поверхности кальцита. [20]
При этом было отмечено уменьшение скорости растворения кальцита за счет сокращения реальной поверхности кристаллов при образовании газовой пленки вследствие уменьшения смачиваемости кристаллов. [21]
Если принять первое объяснение, то неизбежен вывод, что все погребенное органическое вещество превращалось в углеводороды, так как в некоторых случаях пространство, первоначально занятое органическими остатками, теперь почти целиком заполнено нефтью. Даже пустоты, образовавшиеся в результате растворения кальцита, кремнезема или растворимых в воде эвапоритов, содержат жидкие углеводороды. Таким образом, первая гипотеза маловероятна по биологическим и геохимическим причинам. [22]
Растворимость сульфата кальция, который диссоциирует на ионы Са и SO4, непосредственно не зависит от содержания двуокиси углерода в воде. Однако поскольку растворимость карбоната кальция зависит от СОг, то при растворении кальцита концентрация ионов Са может увеличиться настолько, что в воде будет превышено произведение растворимости CaSO4 и гипс может выпадать в осадок. [23]
В книге описаны принципы прогноза и размещения региональных зон нефтегазонакопления в бассейнах седиментации с различной структурно-тектонической, геотермической и фациально-геохи-мической характеристиками, основное внимание-уделено новейшим данным о региональных зонах нефтегазонакопления, контролируемых поясами оптимальных коллекторов. Эти качества автор рассматривает в связи с общей закономерностью разуплотнения верхней части осадочных карбонатсо-держащих комплексов литосферы, которое вызывается растворением кальцита глубже границы его устойчивости. [24]
Отложения, представленные карбонатами кальция, сравнительно эффективно удаляются растворами соляной кислоты. Для защиты металлических поверхностей от коррозии в используемый при этом 5 - 15 % - ный раствор соляной кислоты добавляют ингибиторы коррозии. Растворение кальцита происходит также в результате применения 5 % - ного раствора композиции на основе сульфаминовой кислоты и алкиларилсульфата. [25]
Кривые рис. 3 показывают, что с увеличением числа оборотов мешалки растворение кальцита в серной кислоте в отсутствие поверхностно-активного вещества возрастает. Это обстоятельство находится в согласии с простыми рассуждениями, а именно: с увеличением интенсивности перемешивания увеличивается абразивный эффект, в результате чего ускоряется механическое удаление образующейся на поверхности кальцита пленки CaS04, что связано с освобождением поверхности кальцита и дальнейшим ее растворением. В присутствии добавок растворение кальцита изменяется в крайне незначительных пределах, что, по всей вероятности, можно объяснить экранизацией поверхности кристалла молекулами органического вещества и более прочным Удержанием образующейся на поверхности пленки CaS04 за счет ее стабилизации. Удержание пузырьков газа на поверхности кристаллов в данных условиях затруднительно и вряд ли наблюдаемое явление можно объяснить образованием на поверхности газовой пленки. Результирующий эффект подавления увеличивается с интенсивностью перемешивания только за счет роста растворения кальцита в отсутствие добавок. [26]
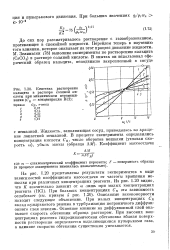 |
Кинетика растворения кальцита в растворе соляной кислоты при механическом перемешивании ( Сн - концентрация НС1. [27] |
Перейдем теперь к изучению того влияния, которое оказывает на этот процесс движение жидкости. Зелиньски 178 ] выполнил эксперименты по растворению кальцита ( СаС03) в растворе соляной кислоты. [28]
При этом начинают происходить коррозия зерен кварца, растворение зерен кварца и полевых шпатов в точках касания друг с другом ( растворение под давлением по принципу Рикке), образование конформных и инкорпорационных контактов между зернами. Одновременно в породах с карбонатным цементом продолжается растворение кальцита. [29]
Сравнивая эту формулу с литературными данными для КГ [1], следует отметить, что КХ отличается от КГ наличием кальция в структуре цеолита и значительно более низким содержанием натрия. На самом деле при данных условиях идет растворение кальцита, являющегося m имесыо к КГ. [30]
Страницы: 1 2 3