Растворение - кристаллогидрат
Cтраница 1
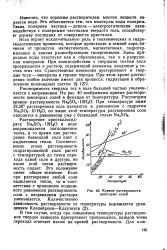 |
Кривые растворимости некоторых солей. [1] |
Растворение кристаллогидрата Na2SO4 10Н2О в воде сопровождается поглощением тепла, в то время как растворение безводной соли идет с выделением тепла. Соответственно этому растворимость гидратированной соли растет с температурой до точки перехода одной соли в другую, но выше этой точки растворимость падает. Это положение имеет общее значение. Если при растворении любой соли выделяется тепло, то в соответствии с принципом подвижного равновесия растворимость соли с нагреванием раствора уменьшается. [2]
 |
Кривые растворимости некоторых солей. [3] |
Растворение кристаллогидрата Na2SO4 10H2O в воде сопровождается поглощением тепла, в то время как растворение безводной соли идет с выделением тепла. Соответственно этому растворимость гидратированной соли растет с температурой до точки перехода одной соли в другую, но выше этой точки растворимость падает. Это положение имеет общее значение. Если при растворении любой соли выделяется тепло, то в соответствии с принципом подвижного 1 равновесия растворимость соли с нагреванием раствора умень - шается. [4]
Энтальпии растворения кристаллогидратов с различным числом молекул воды находятся из табличных значений и используются для вычисления содержания воды в исследуемом образце из энтальпии его растворения. [5]
При растворении кристаллогидрата в воде необходимо учитывать, ято содержащаяся в нем кристаллизационная вода разбавляет раствор. [6]
При растворении кристаллогидрата в воде необходимо учитывать, что содержащаяся в нем кристаллизационная вода разбавляет раствор. [7]
При растворении кристаллогидрата в воде необходимо учитывать, ято содержащаяся в нем кристаллизационная вода разбавляет раствор. [8]
При растворении кристаллогидратов в воде наблюдается более низкий тепловой эффект, чем при растворении безводной соли. [9]
При растворении кристаллогидрата в воде необходимо учитывать разбавление раствора за счет кристаллизационной воды. [10]
При растворении кристаллогидрата в воде необходимо учитывать, что содержащаяся в нем кристаллизационная вода разбавляет раствор. [11]
Обычно процесс растворения кристаллогидратов эндотермичен, а безводных солей - экзотермичен. [12]
Растворы CrF3 получаются растворением кристаллогидрата в воде или гидроокиси хрома в плавиковой кислоте, или восстановлением хромового ангидрида в присутствии HF. Сперанский [8] определил молекулярные веса и электропроводность растворов CrF3 и нашел, что они указывают на незначительную степень электролитической диссоциации. Раствор фиолетовой соли обладает втрое более высокой электропроводностью, чем раствор зеленой соли. [13]
Растворы, полученные растворением кристаллогидратов солей в ТБФ. [14]
Аналогично проводят измерение энтальпии растворения кристаллогидрата. [15]
Страницы: 1 2 3 4