Растворение - никель
Cтраница 1
Растворение никеля идет а поверхности соприкосновения травочного раствора и металла. [1]
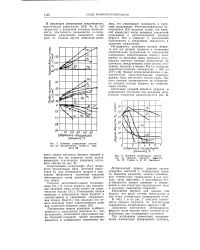 |
Влияние легирующих элементов на механические свойства феррита.| Влияние легирующих элементов на ударную вязкость феррита ( А. П. Гуляев и В. П. Емелина. [2] |
Растворение никеля приводит к измельчению зерна феррита и соответственно к увеличению сопротивления отрыву. [3]
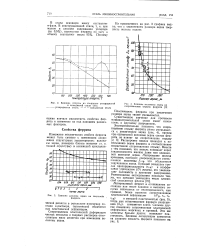 |
Влияние отпуска на твердость углеродистой.| Влияние размера зерна иа твердость феррита. [4] |
Растворение никеля приводит к измельчению зерна феррита и соответственно возрастанию сопротивления отрыву. Вместе с тем показано, что никель понижает порог хладноломкости железа даже при одинаковой величине зерна. Легирование железа кремнием, наоборот, сопровождается уменьшением величины SOTp, что объясняется укрупнением зерна. Кремний повышает предел пропорциональности ( im) и коэффициент упрочнения ( D) железа, что увеличивает склонность к хрупкому разрушению. [5]
Растворение никеля на аноде в аммиачном электролите приводит к образованию комплексного аммиачного иона. Как показали исследования, образованию комплексного иона предшествует возникновение на аноде пленки из продуктов различной степени окисления никеля. Окисление никеля осуществляется за счет разряда ионов гид-роксила, что подтверждает изучение анодной поляризации никеля в рассматриваемом электролите. [6]
Растворение никеля в растворах НС1 и H2SO4 идет с небольшими скоростями, аэрация и повышение температуры растворов значительно увеличивают скорость коррозии. Никель весьма стоек по отношению к щелочам, в том числе разбавленным, при любых температурах, что обусловлено пассивацией. [7]
Растворение никеля в растворах НС1 и HaSO4 идет с небольшими скоростями, аэрация и повышение температуры этих растворов значительно увеличивают скорость коррозии. Он обладает значительной коррозионной стойкостью на воздухе до 900 С, в органических кислотах, в сухом аммиаке и в разбавленных растворах аммонийных и других неокисленных солей. Хлор и хлористый водород при высоких температурах на никель не действуют. [8]
Растворение никеля идет - на поверхности соприкосновения травочного раствора и металла. [9]
На растворение никеля в обоих случаях идет одинаковое количество кислоты. [10]
Скорость растворения никеля при концентрации щелочи 350 г / л КОН, температуре 90 С и плотности тока - 0 25 а / см2 составляет примерно 1 - 2 ми / год. В этих условиях железо растворяется довольно интенсивно. Отсюда был сделан вывод, что наблюдавшаяся ранее коррозия анодной стороны биполярных электродов вызывалась плохим качеством никелевого покрытия и что при тщательном никелировании анодной стороны электрода можно устранить указанную коррозию. Опыт подтвердил, что при хорошем качестве никелирования ( не более 20 пор на 1 дм 1) коррозия выносного листа и основного листа с анодной стороны практически отсутствует и встречается только как исключение. [11]
Для нормального растворения никеля требуется присутствие в электролите ионов хлора; для растворения кобальта нет необходимости вводить активаторы. [12]
При растворении никеля одна молекула серной кислоты взаимодействует с одной молекулой никеля; на 58 7 весовых частей никеля расходуется 98 весовых частей серной кислоты, а на 85 0 кг, никеля 98 - 85: 58 7142 кг 100 % - ной, или 142 - 100: 75 190 кг технической 75 % - ной кислоты. При растворении меди одна молекула серной кислоты взаимодействует с одной молекулой меди. На 63 весовые части меди расходуется 98 весовых частей серной кислоты, а на 28 кг - 98 - 28: 63 43 6 кг. [13]
Возможно ли растворение никеля и выделение хрома при погружении никелевой пластинки в раствор соли трехвалентного хрома. [14]
Анодный процесс растворения никеля существенно влияет на работоспособность никелевых электролитов. При длительном использовании плохо растворимых никелевых анодов выявлено следующее: осадки меняют внешний вид от матового до блестящего; напряжения постепенно переходят от растяжения к сжатию; возникает питтинг; искажаются геометрические размеры копии; подкисляется электролит; получаются твердые и хрупкие осадки. [15]
Страницы: 1 2 3 4